La inteligencia artificial de Google logra un hito frente a uno de los mayores retos de la biología
Un algoritmo que predice la forma de las proteínas a partir de su ADN acelerará la investigación de enfermedades como alzhéimer o diabetes

DeepMind, el laboratorio londinense de inteligencia artificial que Google compró en 2014, ya ha creado programas que ganan siempre al ajedrez, al shogi y al Go, los juegos de tablero más complejos. Pero el objetivo final de la empresa no está en los pasatiempos, sino en resolver acuciantes problemas científicos. Su algoritmo AlphaFold, presentado a principios de diciembre en Cancún, México, ha ganado una competición mundial en predecir la estructura tridimensional de proteínas.
Las proteínas son las máquinas moleculares de los seres vivos. Cada una es una cadena larga de unidades llamadas aminoácidos, como abalorios ensartados en un alambre, que se pliega espontáneamente para adoptar una forma compleja y precisa. La estructura final de cada proteína determina su función. Los anticuerpos, por ejemplo, son como ganchos que se acoplan a los microbios. La hemoglobina tiene un hueco que atrapa moléculas de oxígeno. El colágeno es parecido a un cable trenzado.
Predecir la estructura de cualquier proteína a partir de su secuencia de aminoácidos se considera uno de los santos griales de la biología. No es tarea menor; los aminoácidos son 20 moléculas con propiedades químicas ligeramente distintas, con lo cual están unidos por enlaces de diferentes longitudes y ángulos. Se tardaría más que la edad del universo en doblar una proteína por todas sus configuraciones posibles antes de dar con la estructura tridimensional correcta por azar.
Pese a lo esotérico de este campo científico, es difícil exagerar su importancia. Ciertas enfermedades, como el alzhéimer, el párkinson, la diabetes o la fibrosis quística, se deben a la acumulación de proteínas mal plegadas, algo que se podría evitar conocida la relación entre su secuencia y su estructura. Casi todos los medicamentos actúan por acoplamiento a la región específica de una proteína, un proceso que de nuevo depende de la estructura precisa de la diana. Además, con la capacidad de predecir exactamente cómo se doblará una cadena de aminoácidos, los científicos pueden diseñar proteínas artificiales, por ejemplo para degradar plásticos o compuestos contaminantes, del organismo o del medio ambiente.
En un comunicado, el equipo de DeepMind ha llamado a este logro su “primer hito significativo” en la aplicación de la inteligencia artificial al progreso científico. “El problema del pliegue de las proteínas no está resuelto todavía” advierte Paul Bates, un experto en este campo del Instituto Francis Crick, en Reino Unido, que acudió a la presentación de AlphaFold en Cancún. “El programa de DeepMind acierta más veces y con más precisión que los demás, pero no resuelve todas las estructuras”, explica Bates a Materia. Esto es porque la inteligencia artificial aprende de una base de datos de proteínas conocidas, y por tanto tropieza con estructuras completamente nuevas.
El concurso que ha ganado AlphaFold, llamado Evaluación Crítica de Predicción de Estructuras (CASP en inglés), se celebra cada dos años. En él, cada equipo recibe en intervalos de varios días nuevas secuencias genéticas. Estas se corresponden a proteínas bien estudiadas en el laboratorio, pero cuya estructura no se ha dado a conocer al público. Los concursantes deben aproximarse lo máximo posible con sus modelos de predicción a la forma real de la molécula.
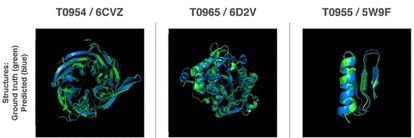
El equipo de Google, que se presentaba por primera vez al certamen, quedó primero de 98 concursantes, al estimar con mayor precisión la estructura de 25 de las 43 proteínas, según informa The Guardian. Para cada secuencia de aminoácidos, suele existir un pliegue correcto, que se corresponde a la configuración de mayor estabilidad bioquímica. En un laboratorio, se puede observar la forma real de las biomoléculas mediante técnicas como la resonancia magnética o la cristalografía de rayos X, un método parecido al que permitió a Rosalind Franklin ver por primera vez la estructura de la doble hélice del ADN.
La inteligencia artificial constituye un avance increíble con respecto a esas técnicas complejas y costosas, aunque todavía no es capaz de sustituirlas por completo. DeepMind entrenó a una red neuronal relacionando la forma y la secuencia génica de miles de proteínas conocidas. Armado con ese conocimiento, el programa AlphaFold predice la distancia y el ángulo entre cada pareja de aminoácidos de la cadena, y luego hace pequeños ajustes a la estructura completa para encontrar la configuración más estable.
Proteins are essential to all known forms of life. Working out how they fold into 3D structures is one of the major outstanding questions in biology and could impact disease understanding, drug discovery, and protein design (2/5) pic.twitter.com/dqe7wdwuJA
— DeepMind (@DeepMind) December 3, 2018
Las aplicaciones médicas más inmediatas de esta tecnología se verán en el diseño de fármacos, incluidos los medicamentos contra el cáncer, opina Bates. “Todavía no se han conseguido modelos con suficiente precisión para esto”, dice. En un futuro algo más lejano, podría llegar la modificación de proteínas asociadas a enfermedades degenerativas como el alzhéimer. “Ya se puede empezar a pensar en esos problemas más difíciles. Esto da un punto de partida".
Los concursantes de DeepMind concluyen que “queda mucho trabajo por hacer antes de poder tener un impacto cuantificable en el tratamiento de enfermedades, la gestión del medio ambiente y otras aplicaciones”, pero añaden que “el potencial es enorme”. Según Bates, el algoritmo ideal probaría cada enlace de la cadena proteica sin necesidad de una referencia externa, pero eso requiere un conocimiento profundo de física inalcanzable todavía. A pesar de que el equipo de DeepMind llega nuevo a una disciplina bien trillada, “lo ha hecho mejor que cualquiera”, asegura el científico británico.


























































