Más transparencia en los ensayos clínicos
La OMS pide a las farmacéuticas que aporten los datos de sus investigaciones a un registro público
La Organización Mundial de la Salud (OMS) va a crear un portal en Internet accesible a pacientes, voluntarios, médicos e investigadores de todo el mundo, cuyo objetivo es recoger todos los ensayos clínicos que se estén realizando. El portal estará listo en pocos meses y permitirá conocer cualquier ensayo con pacientes que se realice en cualquier país. Podrán usarlo voluntarios que quieran contribuir al desarrollo de la ciencia y pacientes que no tengan tratamiento y quieran probar posibles nuevas terapias. "Para el público, estos registros son muy útiles: pueden ir al portal de Internet, seleccionar los ensayos clínicos por enfermedad, ver si se aceptan pacientes, contactar con los responsables e incluso plantearse viajar al país donde se desarrolla el estudio", asegura Ida Sim, coordinadora de la Plataforma Internacional de Registro de Ensayos Clínicos de la OMS.
Los laboratorios niegan datos que pide la OMS alegando que afecta a la competitividad
Unos 9.000 españoles participaron en 2005 en ensayos clínicos de la farmacéutica Novartis
Pero el principal objetivo del registro es aumentar la transparencia de los estudios clínicos. Ahora ya existen registros de ensayos clínicos, muchos promovidos por los propios laboratorios, pero la OMS quiere unificarlos y establecer criterios homogéneos en la recogida de datos. Las farmacéuticas se niegan, por el momento, a facilitar algunos de los que solicita la OMS para el nuevo registro centralizado.
Los actuales registros de ensayos clínicos tienen, según José Sacristán, director médico de Lilly España, una utilidad indiscutible: "Sólo mediante la existencia de una gran base de datos centralizada puede llevarse a cabo lo que se conoce como medicina basada en la evidencia". Permiten evaluar, por ejemplo, si un medicamento es más eficaz que otro, revisando los resultados de los ensayos clínicos publicados. El problema es que no siempre se publican todos los datos.
Para hacerse una idea de la magnitud de los ensayos clínicos en España, valga el siguiente dato: sólo la empresa Novartis implicó a 9.000 personas en este tipo de estudios en el año 2005, según datos de la farmacéutica.
Ningún especialista duda de la utilidad y necesidad de los ensayos clínicos. De hecho, todos los medicamentos que se prescriben fueron probados en su día en miles de voluntarios. Y sociedades científicas como la Sociedad Española de Oncología (Seom) destacan que la participación en ensayos clínicos puede ser de gran utilidad para los enfermos, porque les da opción a recibir tratamientos punteros y un mayor control médico.
Pero no todos los productos que se prueban ofrecen los resultados que se esperan. Algunos tienen además graves efectos adversos. Y cuando los resultados son negativos, no siempre se publican. Casos recientes como el del ensayo clínico de un hospital londinense que acabó con seis voluntarios sanos en la unidad de cuidados intensivos, han arrojado dudas sobre la metodología utilizada en estos experimentos.
La falta de transparencia ha propiciado, según Ida Sim, dos de los escándalos farmacéuticos más notorios de los últimos tiempos. El primero ha provocado una denuncia del fiscal de Nueva York contra la compañía GlaxoSmithKline (GSK) por haber ocultado informes que revelaban un aumento en las tendencias suicidas de adolescentes tratados con Paroxetina (Paxil). En 2004 la farmacéutica aceptó publicar en su sitio de Internet estos informes. En otro juicio en 2001, GSK fue obligada a pagar más de seis millones de euros de indemnización tras considerarse probado que el antidepresivo había sido el responsable del cambio de conducta que llevó a un hombre a matar a varios miembros de su familia.
El segundo gran escándalo todavía se dirime en los tribunales. En 2004, la empresa Merck tuvo que retirar del mercado los medicamentos basados en Rofecoxib (Vioxx, entre otros), al asociarse su consumo con afectaciones cardiovasculares graves e incluso mortales. Cuando fue retirado era uno de los antiinflamatorios más prescritos en el mundo, después de ofrecerse como la panacea que permitía superar los efectos gástricos de los que se utilizaban hasta ese momento.
En ambos casos, recuerda Ida Sim, las compañías ocultaron resultados negativos de los ensayos clínicos previos a la aprobación: "A raíz de estos casos, la comunidad científica y los pacientes comenzaron a plantearse: es posible que las farmacéuticas nos estén ocultando información sobre medicamentos que venden muy caros".
La OMS va a pedir que toda empresa farmacéutica o institución pública que lleve a cabo un ensayo clínico publique 20 datos concretos sobre ellos. Los registros que existen ahora no ofrecen datos homogéneos. La Federación Internacional de Manufacturas y Asociaciones Farmacéuticas (IFPMA) tiene un portal (http://clinicaltrials-dev.ifpma.org, en español) sobre ensayos clínicos y algunas farmacéuticas, como Lilly (www.lillytrials.com), tienen el suyo propio. Lo que pretende el organismo de Naciones Unidas es unificar los criterios y obligar a que se publiquen todos los resultados. "No tiene sentido que las farmacéuticas tengan la opción de incluir o no los ensayos clínicos con malos resultados", sostiene Sim.
Las empresas farmacéuticas, por el momento, no van a acatar las reglas de la OMS. El primer desacuerdo radica en que la OMS quiere que se incluyan en el registro los ensayos clínicos de fase I (los primeros que se hacen en pequeños grupos de pacientes para estudiar la seguridad del medicamento y la pauta de administración). Las farmacéuticas consideran que hacer públicos los resultados de las fases preliminares afecta a la competencia. "Los ensayos clínicos en fase I son estudios muy iniciales. Si publicamos estos datos, otras empresas podrán saber lo que se está haciendo y copiarlo", afirma Yves Juillet, jefe del Comité Regulatorio de la asociación internacional de farmacéuticas IFPMA.
No es el único asunto conflictivo. De los 20 datos que la OMS quiere que figuren, los laboratorios rechazan cinco por considerar que afectan a la competitividad, entre ellos el nombre del científico responsable del ensayo y de la intervención, el número de pacientes, y las variables a medir. "Somos y queremos ser transparentes", afirma Yves Juillet, "pero no vamos a proporcionar los datos de los ensayos en fase I, y decidiremos caso por caso si publicamos esos cinco puntos conflictivos al principio o al final del ensayo", asegura. La OMS considera que es una negativa temporal. "Creo que terminarán facilitando todos los datos. El público sabe lo que está pasando y tanto los pacientes como los médicos van a juzgar a las farmacéuticas por la actitud que adopten", concluye Ida Sim.
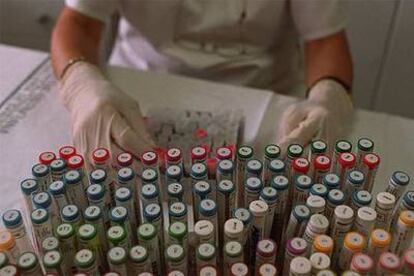
Los ensayos de los laboratorios, más positivos
Los estudios financiados por laboratorios y empresas con ánimo de lucro tienden a presentar resultados positivos en mucha mayor proporción que los realizados por instituciones sin ánimo de lucro, según un estudio publicado el 17 de mayo en la revista JAMA. El estudio, circunscrito a investigaciones sobre medicamentos y dispositivos del ámbito cardiovascular, ha analizado los resultados de ensayos clínicos aleatorios publicados entre los años 2000 y 2005 en tres de las revistas clínicas de mayor impacto: The Lancet, The New England Journal of Medicine y la propia JAMA.
Ya en la década de los noventa, diversos estudios habían puesto de manifiesto que los ensayos financiados por organizaciones con ánimo de lucro tenían más posibilidades de comunicar hallazgos positivos que los subvencionados por organizaciones independientes o sin ánimo de lucro. Se planteó entonces si estas diferencias podían ser debidas a sesgos en el diseño de los ensayos y en la forma de procesar los datos obtenidos.
Paul M. Ridker, del Brigham and Women's Hospital, y José Torres, de la Harvard Medical School de Boston han analizado los resultados de 324 ensayos clínicos cardiovasculares, atendiendo a la fuente de financiación y a si los resultados son favorables al nuevo tratamiento o a la terapia convencional con la que se compara. El 58,6% de los ensayos presentan resultados claramente favorables a los nuevos tratamientos, un 34,6% no plantean diferencias importantes y un 6,8% ofrecen resultados favorables a la terapia habitual.
Pero al agrupar los ensayos en función de su financiación, aparecen grandes diferencias. Entre los ensayos sin ánimo de lucro, 104 en total, el 49% son favorables a los nuevos tratamientos, mientras que el 51% indican que no aportan mejoras sobre la terapia convencional. Entre los ensayos con ánimo de lucro (137 estudios), en cambio, el 67,2% optan significativamente por los nuevos tratamientos, mientras que sólo el 32,8% se inclinan por los ya disponibles o no muestran diferencias significativas. En los financiados conjuntamente por instituciones sin ánimo de lucro y laboratorios, un 54% eran favorables a los nuevos tratamientos.
La desproporción es especialmente acusada en el caso de los estudios destinados a evaluar dispositivos cardiovasculares. En los 38 ensayos aleatorios que los estudiaban, las proporciones en favor de nuevos tratamientos fueron de un 50% en el caso de las organizaciones sin ánimo de lucro; de un 69,2% en el caso de las financiaciones mixtas; y de un 82,4% en el caso de los ensayos con ánimo de lucro."Estos datos parecen demostrar que los incentivos que rodean a las organizaciones con ánimo de lucro pueden influir en los resultados de los ensayos clínicos", sostienen los autores, quienes recuerdan que este tipo de sesgos se ha atribuido "a la parcialidad en el diseño e interpretación de los datos, y a una calidad diferencial de la información". Pero añaden que "existen también otros aspectos que explican parcialmente los resultados observados. Por ejemplo, cuando el primer informe de un ensayo sobre un tratamiento novedoso es nulo o negativo, tiene menos posibilidades de que una fuente de financiación subvencione estudios posteriores. Y cuando el primer ensayo de un tratamiento realmente novedoso es positivo, las probabilidades de que se realicen otros ensayos aumentan" y también que los financien empresas con ánimo de lucro.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.


























































