Científicos europeos simulan el inicio de un embarazo usando un embrión artificial
Los pseudoembriones con células madre humanas pueden abrir una nueva era en la que los humanos dominen las técnicas para generar un bebé o provocar un aborto sin efectos secundarios
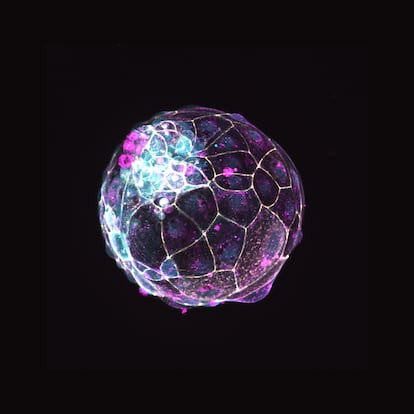

Científicos europeos han creado un embrión artificial a partir de células madre humanas que reproduce en el laboratorio por primera vez un momento crucial del desarrollo humano: cuando el embrión toca por primera vez el útero de la madre y comienza a hacerse sitio para dar lugar a un bebé.
Ese primer contacto se llama implantación y hasta ahora apenas se ha podido estudiar, lo que supone una enorme barrera para entender por qué los humanos somos tan poco efectivos a la hora de reproducirnos, como dice el biólogo Nicolas Rivron, autor principal de este estudio. Rivron, investigador del Instituto de Biotecnología Molecular de Austria, explica que solo la mitad de los óvulos fecundados por un espermatozoide acaban teniendo éxito y dan lugar a una nueva persona. De la otra mitad, muchos de los embarazos frustrados suceden justo durante la implantación. ¿Qué decide que un embrión anide felizmente en el útero de la madre y que otro aparentemente igual desaparezca para siempre? Nadie lo sabe.
El equipo de Rivron ha ideado una forma de simular lo que sucede en el vientre de una madre usando células madre cultivadas en un laboratorio. En un estudio publicado el 2 de diciembre en la revista científica Nature, explica cómo haciendo tres modificaciones moleculares las células madre se reprograman y comienzan a formar esferas muy similares a un embrión de unos siete días de edad, también conocido como blastocisto. En este punto el embrión es una pelota de menos de un milímetro y unas 200 células, pero tiene ya toda la información genética necesaria para generar un ser humano.
“Estos experimentos nos muestran que podemos recrear en una placa de cultivo en el laboratorio el primer contacto entre un embrión y la madreNicolas Rivron
El siguiente paso fue juntar estos pseudoembriones con células de endometrio, que son las que recubren el útero. Los resultados fueron “espectaculares”, celebra Rivron. Si los científicos no hacían nada, nada sucedía, pero si añadían estrógeno y progesterona, hormonas que segregan las mujeres embarazadas, los pseudoembriones se pegaban a las células del útero simulando la ansiada implantación.
“Estos experimentos nos muestran que podemos recrear en una placa de cultivo en el laboratorio el primer contacto entre un embrión y la madre”, ha explicado Rivron en una rueda de prensa para divulgar su estudio. El equipo ha analizado la expresión genética de sus pseudoembriones célula a célula y esta coincide con la de los cigotos humanos reales en un 97%. Otra similitud: solo el 50% de los embriones artificiales se implantan, una tasa igual a la de los humanos.
Este trabajo abre la puerta a que en unos años se controle mucho mejor la capacidad de generar embarazos o de interrumpirlos. “La tasa de éxito de la fecundación in vitro es del 25% aproximadamente. Hay mucho margen para la mejora”, señala Rivron. Una forma de perfeccionar estas técnicas sería analizar la implantación con estos modelos de embrión. Por otro lado, el investigador recuerda que en todo el mundo se producen miles de embarazos no deseados muy problemáticos entre mujeres muy jóvenes. “La mayoría de los anticonceptivos actuales se basan en hormonas, que sirven para prevenir la formación de un embrión o su implantación. Estos tratamientos tienen muchos efectos secundarios y no los pueden usar todas las mujeres, por ejemplo están proscritos para las que sufren cáncer de mama de origen hormonal”, detalla.
El estudio demuestra que una molécula ya conocida —SC144— impide que los pseudoembriones se peguen a las células de endometrio, lo que apunta a que tal vez pueda funcionar como anticonceptivo.
Los científicos solo han permitido que sus embriones artificiales vivan 13 días. Lo han hecho en parte porque en muchos países europeos, incluida España, una ley impide cultivar embriones humanos más allá de los 14 días. La razón es que se piensa que a partir de ese día es imposible que el embrión genere gemelos, por lo que se supone que es justo a las dos semanas cuando aparece un futuro individuo. Ninguna ley impide cultivar embriones artificiales más allá de esta línea roja. Pero Rivron aduce que pasados los 13 días algo se tuerce. El crecimiento de los cigotos de laboratorio comienza a ser más desordenado y diferente al de embriones normales. Es algo que también sucede con los embriones humanos reales cultivados en laboratorio y, de nuevo, nadie sabe por qué.
Esta investigación abre también posibilidades delirantes, como implantar uno de estos embriones artificiales en el útero de un animal o incluso de una mujer e intentar que nazca un bebé. Rivron resalta que “nunca” debería hacerse tal cosa y añade que probablemente no tuviera éxito. Su equipo lleva años intentando implantar un pseudoembrión de ratón en el útero de una ratona. En ninguna ocasión consiguieron generar ratones recién nacidos. “Con toda probabilidad” tampoco funcionaría en humanos, resalta.
“Este es un estudio importante”, resalta Alfonso Martínez-Arias, investigador de la Universidad Pompeu Fabra de Barcelona. “Estos son los primeros modelos embrionarios realmente fiables. Y esto es importante porque permite disminuir y quizás eventualmente eludir el uso de blastocistos humanos derivados de las clínicas de fecundación in vitro para entender el desarrollo humano temprano y sus patologías sin muchas ataduras éticas; aunque la posición ética de estos blastoides es algo que debe discutirse” resalta.
De todos los abortos que suceden, solo el 10% está reconocido clínicamente con una imagen y la constatación de que hay un corazón que latía y ya no lo hace. El resto son pérdidas que suceden unos pocos días antes. Es el iceberg de la pérdida embrionariaMarta Shahbazi, bióloga
El año pasado, Martínez-Arias creó otro modelo de embrión que emula los primeros compases de la gastrulación, un fenómeno que comienza cuando el embrión tiene 14 días y que inicia el proceso de formación del plano general del cuerpo humano. Hasta la aparición de estos modelos, la implantación y la gastrulación humana han sido “cajas negras” casi imposibles de investigar y entender, resalta.
“Este estudio mejora la técnica de creación de pseudoembriones mucho más parecidos a embriones reales y muestra además que estos simulan la implantación, es decir enseñan cómo las células hablan entre sí”, explica Marta Shahbazi, que investiga el desarrollo humano en la Universidad de Cambridge.
El estudio también apunta a caminos alucinantes, como generar miniúteros a partir de las células de una paciente que tiene problemas para tener hijos, implantar en ellos un pseudoembrión y averiguar dónde está el problema. Existe la teoría de que el útero no deja implantarse a los embriones que no son perfectos.
Este momento fundacional de la vida humana es una violenta batalla. El embrión raja la pared del útero y excava un agujero bien profundo para implantarse. Debe camuflarse con señales bioquímicas para que el sistema inmune de la madre no lo aniquile como el ser extraño que es. “De todos los abortos que suceden, solo el 10% está reconocido clínicamente con una imagen y la constatación de que hay un corazón que latía y ya no lo hace. El resto son pérdidas que suceden unos pocos días antes. Es el iceberg de la pérdida embrionaria. La mujer muchas veces ni siquiera sabe que está embarazada. El óvulo fecundado está ahí y tres días después ha desaparecido. ¿Por qué? No lo sabemos”, concluye Shahbazi.
Puedes seguir a MATERIA en Facebook, Twitter e Instagram, o apuntarte aquí para recibir nuestra newsletter semanal.


























































