Un grupo de voluntarios se deja infectar con el parásito de la malaria y acerca el sueño de una vacuna
Una infección controlada en el hígado de 56 personas, seguida de un tratamiento con un fármaco antimalárico, induce una protección de hasta el 100% frente al microorganismo
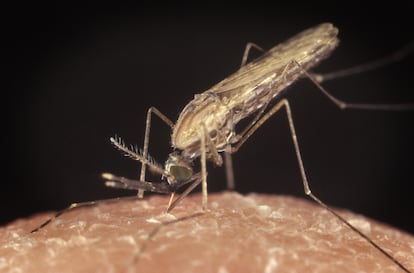

Un equipo científico estadounidense ha infectado a 56 voluntarios con uno de los enemigos más feroces de la humanidad: el parásito de la malaria, culpable cada año de la muerte de unas 420.000 personas, la inmensa mayoría de ellas niños africanos. El audaz experimento ha consistido en inocular a los participantes tres dosis intravenosas de la variante africana del parásito, darles después un fármaco para matar el microorganismo y volverlos a infectar a los tres meses con la misma versión o con una variante brasileña para comprobar que las defensas ya generadas evitan la enfermedad. Los resultados son espectaculares, con una protección de entre el 80% y el 100%, según detalla el médico Patrick Duffy, codirector de la investigación en los Institutos Nacionales de la Salud de EE UU, en la ciudad de Bethesda.
Más de 140 años después de que se identificaran los parásitos responsables de la malaria, todavía no existe ninguna vacuna disponible. La más adelantada es Mosquirix, una inyección de la farmacéutica británica GSK que fue concebida en los años 80 a partir de una proteína del parásito y está en la recta final de los ensayos clínicos. Sus mejores datos muestran una eficacia del 36%. El médico español Pedro Alonso, director del Programa Mundial de Malaria de la Organización Mundial de la Salud, cree que la nueva estrategia acerca el sueño de “una vacuna de alta eficacia que potencialmente abrirá las puertas a la erradicación de la malaria”.
El origen de la nueva estrategia se remonta a finales de los años 60. El microbiólogo británico David Clyde pensó entonces que infectarse con parásitos debilitados podría servir como vacuna contra la malaria. Y probó la idea consigo mismo. La malaria se contrae tras la picadura de una hembra de mosquito, que inocula al ser humano la forma infectiva del parásito. El invasor se dirige en cuestión de minutos al hígado, se multiplica miles de veces en sus células y al cabo de una semana salta a la sangre e infecta los glóbulos rojos, momento en el que aparecen los síntomas de la malaria: fiebre, malestar, dolor de cabeza, diarrea. Clyde y otros colegas recibieron más de 2.700 picaduras de mosquitos previamente irradiados para debilitar los parásitos, logrando una alta protección, pero su estrategia de inmunizar con insectos era obviamente inviable.
El médico estadounidense Patrick Duffy calcula que una vacuna eficaz podría estar lista en cuatro o cinco años
Ya en el siglo XXI, Stephen Hoffman, un antiguo investigador militar de la Marina de EE UU, retomó la idea de Clyde y fundó una empresa para desarrollarla: Sanaria. Hoffman, codirector del nuevo estudio, ha dedicado más de una década a perfeccionar el sistema de producir y conservar el parásito y ya tiene sobre la mesa tres proyectos de vacunas basadas en los parásitos enteros: una candidata en la que los microorganismos están debilitados mediante radiación, otra todavía en pañales con los parásitos atenuados por una modificación genética y una tercera, la publicada ahora, en la que los microbios inyectados se frenan mediante la administración en paralelo de fármacos antimaláricos, como la cloroquina y la pirimetamina. La compañía Sanaria, con sede en Rockville (EE UU), ha recibido 13 millones de euros del Fondo de la Unión Europea para la Malaria.
Pedro Alonso conoce a Hoffman desde hace 35 años y recuerda la noche en la que el estadounidense le contó su idea de intentar vacunar con parásitos completos. “Evidentemente le dije que era una locura”, rememora Alonso, que veía inviable producir cientos de millones de dosis. “La forma infectante del parásito no se podía cultivar entonces, pero Hoffman ha desarrollado un método para cultivar a gran escala los parásitos en los mosquitos, diseccionar sus glándulas salivales, extraer las formas infectantes, preservarlas en frío y que una vez descongeladas sean infectivas. Esto es realmente extraordinario”, aplaude el médico español, que no ha participado en la nueva investigación. Este dominio en la producción de parásitos también ha permitido en los últimos años llevar a cabo algunas infecciones controladas de personas voluntarias.
“Hay un reto logístico gigantesco, que a algunos se les puede antojar inimaginable, que es ir pinchando parásitos vivos a mil millones de africanos y decirles que se tomen un fármaco para frenar su desarrollo”, argumenta Alonso. Para el directivo de la OMS, lo lógico ahora sería modificar genéticamente el parásito para que pueda infectar el hígado y generar defensas, pero sin ser capaz de invadir la sangre y producir la malaria. Así se facilitaría la administración de la vacuna, sin requerir acompañarla de fármacos antimaláricos cuyo olvido podría ser letal. “Esto sí sería un punto de inflexión”, subraya Alonso.
“Lo más importante es que la vacuna funciona incluso contra cepas diferentes del parásito”, aplaude el pediatra Quique Bassat
La bióloga española Sandra March, del Instituto Tecnológico de Massachusetts, firma el nuevo trabajo junto a Patrick Duffy, Stephen Hoffman y el resto de colegas estadounidenses. El equipo de March ha desarrollado un sistema para cultivar el parásito en células del hígado humano, lo que ha permitido estudiar la vacuna experimental en el laboratorio, además de con las 56 personas que se presentaron voluntarias. “Es un grupo pequeño en un ambiente controlado. Ahora hay que esperar a ver qué pasa cuando se empiece a administrar la vacuna a un número mayor de gente en áreas endémicas de malaria”, reconoce March. Sus resultados se publican este miércoles en la revista Nature.
La nueva estrategia alcanzó una eficacia del 100% en los seis voluntarios que recibieron una dosis alta de parásitos y después cloroquina, un fármaco que mata los microorganismos en la sangre. Es la primera vez que una vacuna experimental consigue una protección total durante tres meses frente a diferentes cepas de la malaria, subrayan los autores.
Los investigadores ya han comenzado un ensayo clínico en Malí para confirmar que la vacuna también protege frente a infecciones naturales, protagonizadas a menudo por diferentes variantes del parásito, según explica Duffy. “Si todo va bien —lo que implicaría disponer de todos los recursos necesarios, algo que a menudo no ocurre—, una vacuna muy eficaz contra la malaria podría estar lista para obtener la licencia dentro de cuatro o cinco años, tras realizarse los ensayos necesarios”, calcula el médico estadounidense.
Duffy recuerda que las primeras vacunas contra la covid estuvieron listas en menos de un año. “Quizá en el futuro podamos aplicar esta lección a otros problemas, como la malaria. Para cientos de millones de personas, la malaria es una emergencia que ocurre cada año, y la peor parte se la llevan los niños pequeños y las mujeres embarazadas”, reflexiona.
Una de las razones del fracaso histórico de las vacunas experimentales contra la malaria ha sido la existencia de cientos de cepas diferentes del parásito. El pediatra Quique Bassat recuerda que la propia vacuna de Sanaria con parásitos debilitados por radiación fracasó en condiciones reales en un ensayo en Malí en 2014. El 66% de los vacunados se infectó. “Lo más importante del nuevo estudio es que la vacuna funciona incluso contra cepas diferentes del parásito”, aplaude el investigador, director del Programa de Malaria del Instituto de Salud Global de Barcelona.
El ciclo de vida del parásito es endiablado, con metamorfosis a lo largo de su recorrido desde el mosquito a la sangre humana. Es la primera vez que se demuestra que las formas infectantes en el hígado son capaces de inducir defensas robustas incluso frente a otras cepas. Bassat cree que identificar las proteínas del parásito que generan esa respuesta inmune sería un salto de gigante. “Podrías hacer una vacuna sin ningún riesgo [en comparación con administrar el parásito activo] y sin necesidad de dar un tratamiento antimalárico al mismo tiempo”, destaca.
Puedes escribirnos a manuel@esmateria.com o seguir a MATERIA en Facebook, Twitter, Instagram o suscribirte aquí a nuestra newsletter.


























































