Un mecanismo celular contra el cáncer tutela el inicio de la vida
La senescencia es un proceso determinante del correcto desarrollo embrionario Este procedimiento permite ‘apagar’ las células defectuosas o las que ya no sirven Su presencia no se había descrito nunca en el proceso de gestación humana
Hablar de senescencia era hablar de cáncer o de envejecimiento. Este proceso celular es, junto a la muerte programada, uno de los mecanismos que emplea el organismo para evitar que las lesiones celulares deriven en procesos tumorales. Cuando se detectan fallos en las célula, entra en funcionamiento. La sume en un estado durmiente que le impide multiplicarse y permite que sea eliminada por el sistema inmunitario. Además de estar asociado con el cáncer, también es un fenómeno ligado al envejecimiento: con el paso de los años hay más daño celular y, por ello, mas senescencia; es decir, mayor acumulación de células dormidas que no se replican y que no realizan ninguna función en el tejido o el órgano en el que se encuentran, dificultando su funcionamiento correcto.
Dos trabajos realizados en España publicados este jueves en la revista Cell dan una visión distinta y novedosa (además de mucho más positiva) de la senescencia. Este fenómeno no solo es una reacción a las lesiones celulares y a procesos patológicos, sino que es un elemento central en la regulación de un correcto desarrollo embrionario. Tiene un papel central en el inicio de la vida y la formación del futuro bebé.
“Siempre se había asociado como un mecanismo de defensa frente al cáncer o relacionado con el envejecimiento, pero en el desarrollo del embrión la senescencia ocurre de forma fisiológica, no patológica, es un proceso fundamentalmente beneficioso”, relata Daniel Muñoz-Espín, primer firmante del artículo del Centro Nacional de Investigaciones Oncológicas (CNIO) en el que se describe por primera vez –a partir de trabajos con embriones humanos y de ratón- este proceso en mamíferos. El segundo artículo, de investigadores del Centro de Regulación Genómica de Barcelona, ha llegado a las mismas conclusiones en ensayos en embriones de pollo y ratón.
“Hemos descubierto que la senescencia celular es un mecanismo de remodelación de tejidos durante el desarrollo embrionario”, explica Manuel Serrano, director del grupo de supresión tumoral del CNIO. “El desarrollo embrionario está lleno de procesos de reciclaje: tejidos con una función en una etapa determinada que más adelante se destinan a otra tarea. En este este proceso de rediseño hay células que dejan de ser necesarias, y una forma de librarse de ellas es convertirlas en senescentes”, añade Muñoz-Espín.
Cuando se activa el proceso de senescencia, las células dormidas secretan una serie de moléculas que sirven de reclamo al sistema inmune para que sean engullidas por los macrófagos, células responsables de fagocitar los agentes patógenos del organismo.
Ambos grupos de investigación no solo han demostrado que este proceso de desactivación celular se produce también en el embrión, dino que han identificado el gen que funciona de interruptor del mecanismo y han descrito cómo funciona en algunos tejidos.
Un embrión en pleno desarrollo es una vorágine de células madre en constante replicación y diferenciación. Unos tejidos primigenios dan lugar a otros en una sucesión continua que da desemboca en la especialización celular y el desarrollo de los órganos. En este proceso, hay estructuras que pierden su función y, llegado este momento, deben de ser eliminadas.
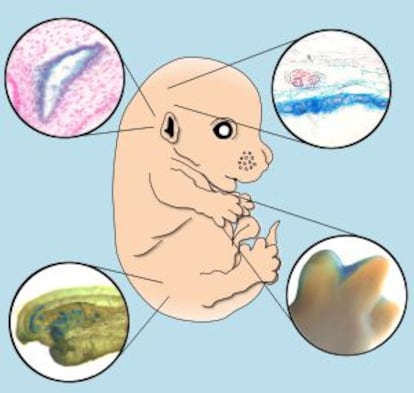
Los investigadores del CNIO se han centrado en dos de ellas para demostrar cómo interviene y que tarea asume la senescencia. Una de ellas es el mesonefros, un tejido que asume la función renal mientras los riñones se están desarrollando. Cuando los órganos definitivos ya están formados, este tejido pierde su sentido, involuciona y prácticamente desaparece. Lo único que queda de él es una especie de tubo que acaba formando los conductos deferentes y que interviene en la formación de la vagina.
El responsable de todo ello –de la activación de la senescencia y, en este caso, de la desaparición del mesonefroses- es el gen p21, que actúa como un interruptor para poner en marcha el proceso. Para comprobarlo, los autores del trabajo eliminaron el p21. “Se pusieron en marcha procesos compensatorios ya que el programa de embriogénesis es muy robusto y tiene mecanismos alternativos”, advierte Muñoz-Espín, “sin embargo, detectamos problemas en la correcta formación de la vagina”.
Los investigadores del CNIO también observaron este mismo proceso en otra estructura embrionaria: el saco endolonfático, situada en el oído interno. Sus colegas del CRG de Barcelona se centraron en la desaparición de la membrana que une los dedos en las primeras etapas del desarrollo embrionario y el cierre del tubo neural.
En todos estos casos, el gen regulador era también el p21. Los autores confían en que después de este primer trabajo se detecte este proceso de senescencia programada en "otros muchos procesos del desarrollo embrionario".


























































