El panel de expertos de la agencia del medicamento de EE UU desaconseja administrar la tercera dosis de la vacuna contra la covid
El grupo de científicos concluye que no hay evidencia suficiente ni una necesidad imperiosa para que los adultos sanos reciban una tercera dosis

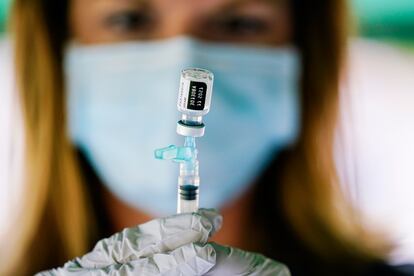
Un panel de expertos que asesora a la agencia reguladora del medicamento en Estados Unidos (FDA, por sus siglas en inglés) ha recomendado este viernes no aprobar una inyección de refuerzo de la vacuna contra el coronavirus de Pfizer-BioNTech a los mayores de 16 años. El comité, que parecía bastante dividido durante el debate, decidió por 16 votos en contra y solo 3 a favor de aprobar la tercera dosis. Por unanimidad, los expertos sí dieron luz verde a una inyección adicional para los mayores de 65 años y personas con un alto riesgo de enfermedad grave. La FDA, que no está obligada a seguir los consejos del comité asesor, pero que suele seguirlos, dará a conocer su decisión en los próximos días.
La sorpresiva decisión trunca los planes de la Administración de Joe Biden que esperaba poner en marcha las vacunas de refuerzo para atajar la propagación del virus debido a la variante delta. A mediados de agosto, el presidente estadounidense anunció un plan para ofrecer la dosis de refuerzo a la población general inmunizada con Pfizer-BioNTech y Moderna a partir del 20 de septiembre -los pacientes inmunodeprimidos ya pueden recibir una tercera inyección-. Varios expertos en salud consideraron que el anuncio del mandatario era prematuro y lo criticaron por hacer público el aviso antes de que la FDA tomara una decisión sobre si era conveniente, basándose en la evidencia disponible. Sin el visto bueno de la agencia, la Casa Blanca tiene las manos atadas.
Biden aseguró que los vacunados podrían pincharse por tercera vez ocho meses después de haber recibido la segunda dosis. Sin embargo, la farmacéutica Pfizer-BioNTech solicitó a la FDA que el plazo fuera solo de seis meses. La opción de dar el visto bueno a una tercera inyección de la vacuna de Moderna se ha retrasado.
A pesar de que todavía existe una mínima posibilidad de que la FDA apruebe la dosis de refuerzo, la agencia no es la que zanja el tema. Los expertos de los Centros para el Control y Prevención de Enfermedades (CDC, por sus siglas en inglés) se reunirán el próximo miércoles y jueves para definir, entre otras cosas, quiénes y cuándo podrían recibir una tercera ronda de inyecciones. Por ahora se han mostrado abiertos a una dosis de refuerzo para los adultos mayores, los residentes de hogares de ancianos y los trabajadores de atención médica de primera línea.
La discusión de los asesores de la FDA se centró este viernes en aclarar si la caída en la efectividad de las vacunas puede llevar a un aumento de los casos graves de covid entre los inoculados. La diversa interpretación de los datos marcó el debate, que se prolongó durante toda la mañana. “Sabemos que puede haber diferentes opiniones al interpretar los datos”, sostuvo el doctor Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA, quien reconoció que “son complejos y están en evolución”.
La información presentada por la doctora Sara Oliver, de los CDC, reveló que las dos dosis de la vacuna siguen evitando la covid grave, incluso en los mayores de 75 años. “En este momento, está claro que los no vacunados están impulsando la transmisión en EE UU”, añadió la doctora Amanda Cohn, también de los CDC.
Por su parte, los expertos israelíes, apoyados en su propia experiencia, aseguraron que la dosis de refuerzo redujo drásticamente los casos graves provocados por la variante delta. Israel aprobó en julio la tercera inyección de Pfizer-BioNTech. Un estudio que analizó los resultados de esa decisión arrojó que los mayores de 60 años que recibieron una dosis de refuerzo tenían un riesgo 11 veces menor de infectarse que las personas a las que no se les inoculó el tercer pinchazo, según la investigación publicada el miércoles en New England Journal of Medicine. Si bien el debate de este viernes en EE UU abordaba solo a Pfizer-BioNTech, la decisión era mayúscula, ya que marca el recorrido de las otras vacunas aprobadas en la potencia mundial.
Los principales funcionarios federales de Salud de EE UU, incluido el doctor Anthony Fauci, asesor médico en jefe del presidente Biden, llevan semanas alertando de que la inmunidad decae entre los inoculados con la pauta completa y que ya hay indicios de un retroceso en la eficacia para proteger a los inoculados en los casos graves, lo que puede derivar en un aumento de las hospitalizaciones. De las tres vacunas disponibles en EE UU, Moderna es la más efectiva (93%) para evitar que las personas acaben en el hospital, según un estudio de los CDC publicado este viernes, aunque el único fármaco que cuenta con la aprobación completa de la agencia de medicamentos es Pfizer-BioNTech.
La Organización Mundial de la Salud (OMS) se ha opuesto a que los países más ricos administren una tercera dosis cuando los más pobres aún no cuentan con vacunas suficientes para inmunizar por primera vez a su población elegible. Dos importantes revisores de vacunas de la FDA firmaron este lunes junto a un grupo de científicos internacionales un artículo en The Lancet, donde rechazaban la necesidad de refuerzos en personas sanas debido a la falta de evidencias. Ambos van a renunciar a la agencia reguladora. Una de ellas, la doctora Marian Gruber, intervino esta mañana en el panel: “Todas mis acciones y decisiones a lo largo de mis 32 años de carrera en la FDA se han basado en la ciencia”.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.




























































