El dictamen de la EMA sobre la vacuna de AstraZeneca agita la inmunización europea
España, Italia y Bélgica se apresuran a limitar la población a la que se administrará el fármaco, mientras que otros países siguen estudiándolo

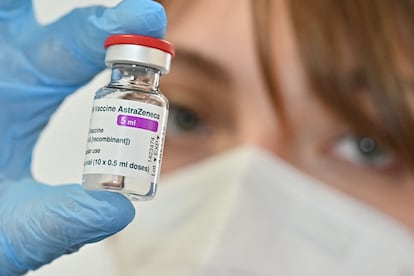
La farmacéutica AstraZeneca deberá advertir finalmente de que entre los “efectos secundarios muy raros” de su vacuna contra la covid-19 está la “inusual” posibilidad de que genere trombos. Empleando la máxima prudencia, la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) concluyó el miércoles que sí existe una relación entre el fármaco y los casos de coágulos sanguíneos detectados en ciudadanos de la Unión Europea a quienes se les había administrado la vacuna. El dictamen, que pone énfasis en la “elevada efectividad” de la vacuna para salvar vidas, ha provocado un nuevo vuelco en los criterios que emplean los países de la UE para sus campañas de vacunación. España, Italia y Bélgica decidieron imponer nuevas restricciones tras una reunión por videoconferencia de los 27 ministros de Sanidad.
El informe de la EMA es el resultado de una investigación en profundidad de 86 casos de trombos reportados por las autoridades nacionales hasta el 22 de marzo, de los cuales 18 acabaron en fallecimiento. 62 trombos eran cerebrales y 24 abdominales. Con posterioridad a esa fecha, los países siguieron llevando casos a la EMA, de modo que hasta el 4 de abril pasado se habían registrado 222 casos en toda la UE. Hasta ese día, 34 millones de personas habían sido vacunadas en los países del Espacio Económico Europeo y el Reino Unido.
De las conclusiones del Comité de Evaluación de Riesgos de Farmacovigilancia dependía buena parte de la estrategia de vacunación de los 27 socios de la UE, puesto que la agencia dejó la aplicación del dictamen en manos de los Estados. Países Bajos, Alemania o Finlandia habían decidido restringir el uso de la vacuna de AstraZeneca a ciudadanos de 60 años o más, puesto que la mayoría de los casos se habían producido en mujeres menores de esa edad. La EMA, sin embargo, no ha podido confirmar aún que los factores de edad, sexo o historial médico sean determinantes para sufrir coágulos. Es más, los expertos de la agencia han razonado que dado el uso distinto que se está dando a esa vacuna en cada país —con una mayor administración a mujeres de esa edad—, no se puede concluir que ese grupo tenga un riesgo superior al resto.
A pesar de que la EMA ha insistido en que no podía establecer una capa de población más vulnerable, varios países (entre ellos, Bélgica, España e Italia) se han decantado por ser más cautos con el uso del suero de AstraZeneca. Previendo los efectos que el dictamen de la EMA podía tener sobre la campaña de vacunación, la presidencia de turno de la UE, en manos de Portugal, convocó una reunión ministerial para tratar de acordar una posición que diera “confianza” en la ciudadanía europea, que hasta ahora ha visto cómo las capitales han hecho de los criterios de vacunación un extraño galimatías.
También la Comisión Europea ha tratado de alentar una respuesta coordinada. En la reunión en la que los 27 socios han puesto en común las decisiones que barruntaban, la comisaria europea de Sanidad, Stella Kyriakides, ha advertido a los ministros de que si bien las decisiones que adopten iban a ser políticas, estas debían basarse en “una evaluación científica de los riesgos y beneficios”. “Es esencial que sigamos un enfoque coordinado europeo. Un enfoque que no confunda a nuestros ciudadanos, y que no encienda los recelos de las vacunas, que esté basado en la ciencia”, ha afirmado.
Más investigación
Sin embargo, Bélgica no ha esperado ni al término de esa reunión para anunciar que iba a restringir la administración de la vacuna a mayores de 55 años, como ya hace actualmente Francia. Después de la reunión, España e Italia han informado de que dispensarían el fármaco de la compañía anglosueca a mayores de 60 años, siguiendo los pasos de Alemania, Países Bajos y Finlandia.
Esos cambios de criterio que puedan adoptar los países supondrán nuevos ajustes en una campaña de vacunación europea que, tras un primer trimestre al ralentí por los incumplimientos de AstraZeneca, empezaba a cobrar ritmo. A pesar de que el miércoles solo el 6,4% de la población europea había recibido la pauta completa de inmunización, desde la Comisión se baraja mediados de julio como la fecha en la que el 70% de la población adulta podría estar vacunada si se cumplen a rajatabla las entregas.
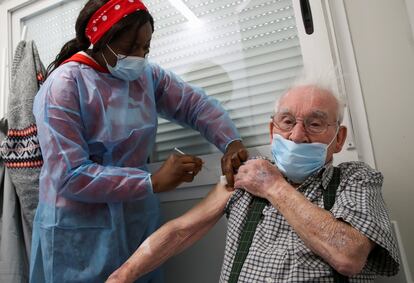
Los expertos de la EMA sostienen que seguirán investigando los efectos secundarios de esa vacuna, para los que de momento no hay tratamiento. Ahora bien, respaldan el uso de un medicamento que se ha demostrado “altamente eficaz”, en palabras de la directora ejecutiva de la EMA, Emer Cooke, y que prácticamente impide que la covid-19 evolucione a una fase grave. “El riesgo de mortalidad por la covid-19 es mucho mayor que la mortalidad por estos efectos secundarios muy raros”, ha sostenido Cooke en una rueda de prensa desde Ámsterdam.
El mensaje de la EMA fue claro: hay un vínculo entre los trombos detectados y la administración de la vacuna de la farmacéutica anglosueca, pero se trata de casos muy raros y los beneficios de la vacuna siguen primando. “La covid-19 es una enfermedad muy grave, y la vacuna es efectiva evitando la enfermedad, la hospitalización y la mortalidad. En su conjunto, el beneficio es superior al riesgo”, ha abundado Sabine Straus, jefa del comité de Seguridad de la EMA. La decisión se tomó tras haber estudiado también informes de expertos independientes.
Más prudente que la EMA fue la Organización Mundial de la Salud, que ha considerado que es “plausible, pero no confirmado” el vínculo entre la vacuna y los tromboembolismos registrados. La farmacéutica ha destacado en un comunicado que los exámenes de las agencias británica y europea “reafirmaron que la vacuna ofrece una protección de alto nivel contra todas la formas graves de covid-19 y que esos beneficios continúan superando ampliamente los riesgos”. El medicamento de AstraZeneca fue el tercero en recibir la autorización de la EMA y la Comisión Europea para salir al mercado. Antes lo habían hecho las vacunas de Pfizer-BioNTech y Moderna, y después la de Janssen.
El dilema de los países de la UE
En todo caso, el ministro de Sanidad de Países Bajos, Hugo de Jonge, ha expresado lo que en estos momentos está sobre la mesa de todos los países. De Jonge ha dicho que la vacunación con AstraZeneca es “un dilema para todos los Estados miembros” de la UE, puesto que los hace elegir entre proteger al máximo de “los riesgos para la salud debido a los efectos secundarios muy raros” de coagulación sanguínea y los “efectos de aplazamiento” que puede tener para los países prescindir de esta vacuna para esa parte de la ciudadanía. “La seguridad debe estar fuera de toda duda”, ha remachado.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.




























































