Aissam, el niño que escapó de un mundo en silencio gracias a la terapia génica: “¡Estoy oyendo el teléfono!”
El menor, de 12 años, es la primera persona en Europa y Estados Unidos con una sordera congénita que vuelve a oír gracias a una terapia génica: ha recobrado audición, aunque probablemente nunca podrá desarrollar el lenguaje

Una burbuja de silencio absoluto ha cobijado al niño Aissam Dam durante toda su vida. Once años en la penumbra de un mutismo tajante. Ni una palabra, ni un grito, ni una voz habían atravesado nunca los muros de esa rara sordera congénita que ha marcado su vida desde que nació. En su Marruecos natal, nunca aprendió a escribir ni a leer, apenas fue al colegio y se comunicaba con su familia por gestos, en un lenguaje de signos no reglado, solo para darse a entender. Así vivió hasta que unas cuantas carambolas de la vida, una novedosa terapia génica y varios miles de kilómetros de por medio lo llevaron, de la mano del Hospital Sant Joan de Déu de Barcelona, hasta un centro sanitario infantil de Filadelfia, en Estados Unidos, donde la ciencia le alumbró, por primera vez, el mundo de los sonidos. Su madre, Naima Tbir, recuerda emocionada aquel día, hace apenas siete meses: “El primer día después de la cirugía, el padre nos hizo una videollamada con él y el niño me dijo [con signos]: ‘¡Estoy oyendo los sonidos del teléfono!”.
Aissam se ha convertido en la primera persona en el mundo occidental (Europa y Estados Unidos) en recibir una terapia génica para tratar una sordera congénita. Y su caso, además, ha sido un éxito: ha recuperado la audición e identifica sonidos, aunque sus médicos advierten de que, por su edad, ya es tarde para aprender el lenguaje y probablemente, nunca podrá hablar con fluidez.
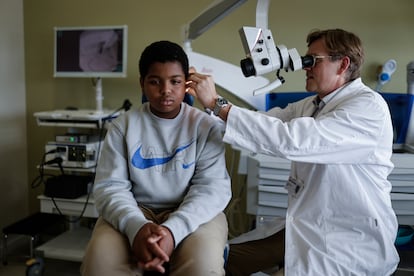
Por los pasillos coloreados del Sant Joan de Déu, Aissam arrastra los pies cabizbajo. Está enfadado. No tiene ganas de fotos, ni de preguntas, ni de revisiones médicas. Aguanta el tipo, enfurruñado, mientras su doctor, Oliver Haag, jefe de Otorrinolaringología del hospital, inspecciona su oído derecho, pero no tiene muchas ganas de cuentos. “Está enfadado porque quiere ir al colegio, no quiere perder ni un rato de clase”, explica su madre a través de una traductora que la acompaña. El mundo de sonidos que se le ha abierto al chaval, que ya ha cumplido los 12 años, le ha dado una nueva vida y hasta el colegio se ve distinto: “Aissam nació sordo. Lo supimos porque tenemos dos hijos mayores que tampoco oyen ni hablan. Fue un año al colegio en Marruecos, pero no entendía nada”, lamenta Naima.
El niño padecía una enfermedad muy poco frecuente, una sordera causada por una mutación en el gen otof, clave para la audición. “Es una mutación de herencia autosomal recesiva, por eso hay familias con varios hijos afectados. Los padres pueden ser portadores sanos, pero si a los hijos les toca la mutación por parte de ambos padres, padecen de la enfermedad”, expone Haag. Apenas 20.000 personas en Europa la padecen: “El gen otof codifica la otoferlina, una pequeña proteína de las células dentro de la cóclea que transmiten el sonido en el líquido de la cóclea”, explica Haag. En un oído sano, el sonido avanza como ondas de aire hasta que llega a esa especie de caparazón de caracol que es la cóclea. Ahí, las ondas se transmiten a través del líquido que baña el interior de esta caracola hasta el nervio auditivo: en concreto, en ese mar coclear, hay unas células sensoriales con pelillos (células ciliadas) que funcionan como sensores de las vibraciones que provoca el sonido y se encargan de transmitir el estímulo sonoro al cerebro. “La otoferlina es una de esas proteínas que, si no funciona bien, impide a la célula ciliada transmitir el estímulo de forma correcta. No funciona la estimulación del nervio. Queda interrumpida la cadena y la información no llega al cerebro de forma correcta. Pero si se repara ese gen, esa proteína, vuelve a funcionar toda la cadena”.
Aissam y su familia se mudaron junto a Barcelona en 2018. El padre, que había migrado a España 19 años atrás, logró completar un proceso de reagrupación familiar y el pequeño, junto a su madre y sus hermanos, se reunió con él en la capital catalana. Volvió a la escuela y allí, “gracias al personal del colegio y a una amiga marroquí con un hijo con un problema parecido”, cuenta Naima, entraron en el circuito asistencial del Sant Joan de Déu para tratar su sordera.
Un estudio genético confirmó esa mutación en el gen otof y, mientras el pequeño seguía con sus visitas y controles en el hospital, el equipo de Haag se embarcó en un estudio internacional para escudriñar en la historia natural de esta misma enfermedad. Esa investigación fue el germen de la terapia génica que luego se desarrolló y Aissam resultó ser un caso especialmente paradigmático que iba como anillo al dedo para toda la revolución científica que se estaba gestando.

“Aissam era un caso particular porque tiene esta mutación, tiene una sordera y no tiene un implante coclear”, explica Haag. Es un perfil poco frecuente en los países occidentales, donde este tipo de patologías se suelen tratar en la primera infancia con un implante que les permita recuperar capacidad auditiva. “En nuestro ámbito, la mayoría de estos pacientes lleva un implante coclear y esto excluye la posibilidad de recibir terapia génica. Tiene que cumplir de tener una mutación muy rara y tener todavía funcionando unas células dentro de la cóclea para hacerle posible candidato”, relata el otorrinolaringólogo.
Cumplía las características y, con el favor de la familia y el aval médico, se embarcó en el ensayo clínico para validar una nueva terapia génica que pretendía devolver la audición al pequeño. La técnica consiste en introducir en las células ciliadas, a través de un virus no patógeno (no es dañino) que funciona como “caballo de Troya”, ejemplifica Haag, las instrucciones correctas para solventar el fallo con el que nació el chaval. “Hay una información genética defectuosa que hace que esta proteína no se produzca de forma correcta. Pues, lo que se hace es una transferencia genética: se lleva información genética correcta que llega a los núcleos de las células y se repara este defecto en la producción de este proteína, para que a partir de ahí se puede producir de forma correcta. Y con esto recuperar la audición”, relata su médico.
Aissam viajó con su padre y Haag al Hospital Infantil de Filadelfia donde se sometería a la nueva terapia. La intervención, que se hizo solo en el oído derecho, duró un par de horas, aunque el niño se quedó en la ciudad durante tres meses para someterse a un seguimiento exhaustivo.
Según la familia, el pequeño ya empezó a percibir sonidos pronto. Como los ruidos que salían del móvil cuando el padre hizo la primera videollamada a la familia en España. Cuenta su madre que, en una de las primeras impresiones al percibir sonidos, el niño, “en un ademán que significa gracias a Dios”, juntó las manos dibujando una especie de cuenco y expresó con gestos: “¡Ahora estoy escuchando mucho mejor que antes!”.
Al mes de la intervención, en las primeras audiometrías y estudios médicos, el éxito de la intervención era evidente. “Este primer ensayo iba, sobre todo, para mirar la seguridad del paciente, el funcionamiento de todos los aparatos de aplicación, por eso se empieza con dosis bajas. No se sabía si esta dosis ya era la suficiente o si se tenía que subir. Ha sido un poco experimental. La sorpresa ha sido que ha funcionado muy bien, ha recuperado en poco tiempo, en menos de un mes, ya un 80% de la audición: en las frecuencias graves tiene una pérdida leve, pero en las frecuencias agudas tiene una audición normal, a 20 decibelios. Ha pasado de una sordera profunda a una audición casi normal. Es un cambio muy grande. Antes no escuchaba nada y ahora, cuando le llamas se gira, escucha cómo suena un coche o cuando le cortan el pelo, dice que son cosas que antes nunca había sentido”, explica Haag.
Dificultades con el lenguaje
El niño ya emite sonidos e incluso ha aprendido a decir su nombre, pero los médicos ven poco probable que pueda desarrollar el lenguaje. La terapia génica le ha permitido salir de ese mundo en silencio, pero llega tarde para devolverle el aprendizaje del habla. “Todo lo que se trata después de estos tres primeros años de vida y de desconexión entre oído y cerebro, los resultados empeoran mucho porque se ocupa el cerebro con otras cosas y las vías auditivas ya no se desarrollan de la misma manera”, lamenta Haag. También influye cuánto se trabaja y se estimula desde pequeño, porque hay pacientes pediátricos sordos “que pueden ser locutivos y hablar”, agrega. Pero no es el caso de Aissam. “Si no se hace esto, pues no hay lenguaje ni comprensión. Y ahora él tendrá la entrada auditiva, pero sí la conexión entre la cóclea y el cerebro no está trabajada y tampoco tiene en el disco duro, en el córtex del cerebro, un espacio dedicado a audición e integrado ahí, irá mejorando lo que oye o entiende, pero no será suficiente. Aunque notará mejoría”, expone el médico.
Ya la nota, de hecho. El niño y todos a su alrededor. El propio Haag insiste en que es “un niño muy dispuesto, muy simpático” y, “aunque no ha sido trabajado, no ha recibido una rehabilitación auditiva ni ha sido enseñado”, aprenderá. “Ahora está escolarizado, tiene el lenguaje de signos y también se puede apoyar en sus sensaciones auditivas. Y seguramente, aunque la neuroplasticidad es importante en los primeros años de vida, él, a lo largo de su vida, seguirá aprendiendo e interpretando lo que oye”. Aissam juega al fútbol, va a la piscina y le encanta el colegio, un centro adaptado para niños con necesidades educativas especiales en Santa Coloma de Gramenet. La madre es contundente: “Está muy contento”.
Aissam es el principio de una revolución terapéutica que, de consolidarse, puede cambiar el paradigma asistencial en este tipo de pacientes o en otros con sorderas por errores genéticos más prevalentes. En su mismo estudio hay un niño más tratado en Taiwán y dos más para tratar en Estados Unidos. Otro estudio, de investigadores chinos, también ha mostrado resultados con una técnica similar. La idea de los científicos, con todo, es llevar esta terapia génica a edades más tempranas para no perder esa ventana de oportunidad y aprendizaje del lenguaje en los primeros años de vida y que el impacto sea el menor posible.
Haag se muestra entusiasmado con el potencial de estos tratamientos, pero baja los pies a tierra y apela a la cautela: “Es un comienzo con un gen en un oído solo. Hay que ajustar las expectativas”, avisa. Falta por saber el impacto a largo plazo o cuándo y cómo es mejor aplicar esta técnica, por ejemplo. El médico pide, sobre todo, no renunciar a otros tratamientos, como el implante coclear, a la espera de una terapia génica como esta que, por ahora, solo es experimental: “Las expectativas globales son buenas y muy interesantes, pero no está aquí todavía”, conviene.
Puedes seguir a EL PAÍS Salud y Bienestar en Facebook, X e Instagram.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.




























































