Córneas hechas con colágeno de cerdo devuelven la visión a una veintena de personas
Una investigación piloto con tejidos corneales creados a partir de bioingeniería abre la puerta a una alternativa al trasplante de córnea humana, un tejido escaso en países de medios y bajos ingresos

La ciencia ha abierto una nueva puerta para tratar la ceguera corneal, que se produce cuando esa membrana transparente que recubre el frente del ojo y actúa como lente, se vuelve opaca e impide que la luz llegue al fondo del ojo, impidiendo la visión. Aunque puede tener cura a través de un trasplante, los expertos estiman que hay 12,7 millones de personas esperando una córnea donada y estas membranas escasean: hay una disponible por cada 70 necesarias. Así, con la atención puesta, sobre todo, en países donde la donación de córneas humanas es más escasa por la limitada infraestructura para la donación, recolección y guarda en bancos de tejidos, un grupo de investigadores suecos ha probado, en un estudio piloto cuyos resultados se han publicado en la revista Nature Biotechnology, unas córneas hechas con colágeno de piel de cerdo en 20 personas con estos tejidos enfermos (todos ciudadanos de Irán o la India, 14 de ellos ciegos). A los dos años, todos los pacientes habían mejorado y los que estaban ciegos, podían ver. Aunque serán precisos ensayos clínicos más complejos para validar la medida, la primera prueba con este tejido corneal creado por bioingeniería ha demostrado que es seguro.
La ceguera corneal también tiene una vertiente socioeconómica: la incidencia es de un millón de nuevos casos al año, pero se concentra, sobre todo, en países de ingresos bajos y medios de Asia, África y Oriente Próximo, explican los investigadores. Precisamente, donde más difícil es conseguir una córnea humana donada, por un sinfín de “barreras económicas, culturales, tecnológicas, políticas y éticas”. Encontrar una alternativa era clave, señalan los autores, para poder combatir el queratocono, una enfermedad que afecta a esta membrana, debilitándola y adelgazándola, y que resulta la causante de la mayoría de los casos que precisan de un trasplante.
Para encontrar una alternativa a la córnea humana donada, los investigadores tiraron de bioingeniería con el colágeno, principal proteína de la córnea humana, como materia prima. “Para un suministro abundante, pero sostenible y rentable de colágeno, utilizamos colágeno de grado médico procedente de piel porcina, un subproducto purificado de la industria alimentaria que ya se utiliza en dispositivos médicos aprobados por la FDA [la agencia reguladora estadounidense] para la cirugía de glaucoma y como vendaje para heridas”, explican en su artículo. A diferencia de las córneas donadas, que deben usarse en menos de dos semanas, las membranas obtenidas por este sistema, se pueden almacenar durante dos años, lo que también facilita la operativa de almacenamiento e implantación.
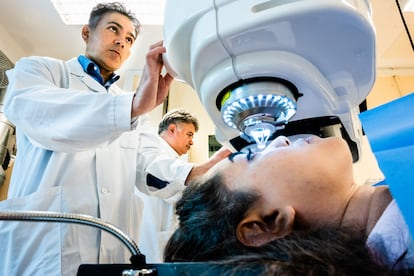
Los investigadores emplearon, además, una técnica de implante mucho menos invasiva que la habitual, que requiere suturas quirúrgicas y solo se puede hacer en grandes hospitales. “Se podría utilizar un método menos invasivo en más hospitales, ayudando así a más personas. Con nuestro método, el cirujano no necesita extirpar el propio tejido del paciente. En su lugar, se hace una pequeña incisión, a través de la cual se inserta el implante en la córnea existente”, apunta en un comunicado de la Universidad de Linköping, Neil Lagali, profesor del Departamento de Ciencias Biomédicas y Clínicas en esa institución y uno de los autores del experimento.
Mejora de la visión
Durante los dos años de seguimiento de los pacientes —la mayoría ciegos antes de recibir el implante— no se observaron efectos adversos ni complicaciones. Los resultados, apuntan los investigadores, son similares a los de un trasplante de córnea humana y se aprecia una mejora de la agudeza visual: el tejido sanó rápido y solo fue necesario, según los autores, ocho semanas de colirio inmunosupresor para evitar el rechazo al implante. De los 14 participantes que estaban totalmente ciegos antes del experimento, todos recuperaron parcial o totalmente la vista tras el trasplante.
La seguridad y la eficacia han sido “el núcleo del trabajo”, añadió en el mismo comunicado, Mehrdad Rafat, director ejecutivo de la empresa LinkoCare Life Sciences AB, que fabrica las córneas creadas con bioingeniería utilizadas en el ensayo: “Hemos realizado importantes esfuerzos para garantizar que nuestro invento esté ampliamente disponible y sea asequible para todos y no solo para los ricos. Es por eso que esta tecnología se puede utilizar en todas partes del mundo”.
Antes de llegar al mercado, esta opción terapéutica tendrá que pasar por más pruebas para validar su eficacia. “Los resultados muestran que es posible desarrollar un biomaterial que cumpla con todos los criterios para ser utilizado como implantes humanos, que pueda ser producido en masa y almacenado hasta por dos años, y así llegar a más personas con problemas de visión. Esto nos ayuda a sortear el problema de la escasez de tejido corneal donado y el acceso a otros tratamientos para enfermedades oculares”, concretó Lagali.
La investigación publicada en Nature Biotechnology arroja luz para combatir las desigualdades en el acceso al trasplante de córnea, pero no es la primera vez que se intenta buscar alternativas a las córneas humanas donadas: hace más de una década, por ejemplo, investigadores españoles se sumaban a la carrera en busca de córneas artificiales a partir de células madre de la córnea extraída de un donante cadáver para paliar los problemas visuales. La lucha contra la ceguera, con todo, se juega hoy también en otro plano: el de la optogenética, la terapia génica con proteínas fotosensibles que ya se ensaya en humanos y ha logrado devolver parcialmente la visión a una persona tras 40 años de ceguera. La investigación con el uso de células madre para combatir la pérdida de visión también sigue en marcha y ya se ha logrado demostrar, en estudios preliminares, que injertar estas células en la retina no causa rechazo y permite revertir daños incurables.
Puedes seguir a MATERIA en Facebook, Twitter e Instagram, o apuntarte aquí para recibir nuestra newsletter semanal.


























































