Las seis alternativas de vacuna que baraja Europa contra el coronavirus
La UE tiene un solo contrato cerrado, con AstraZeneca-Oxford, pero otros cinco preacuerdos para comprar, cuando estén listas, 1.205 millones de dosis
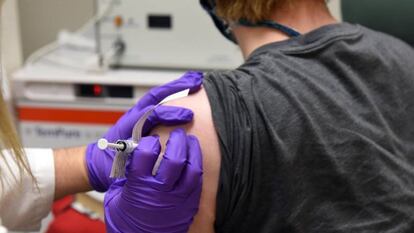
El camino hacia la vacunación contra el coronavirus es esperanzador, pero incierto: ningún medicamento ha demostrado todavía eficacia y seguridad en un amplio número de personas (lo que se conoce como fase 3), pero varios están cerca de conseguirlo. La Unión Europea está en conversaciones muy avanzadas con cinco empresas, tras anunciar este miércoles un preacuerdo con el consorcio formado por BioNTech y Pfizer para adquirir al menos 200 millones de dosis cuando esté lista la vacuna. Pero solo ha cerrado el contrato con una: AstraZeneca, que este miércoles ha suspendido temporalmente sus ensayos por un efecto adverso que tendrá que estudiar.
“Era parte del guion previsto. Detectar este tipo de situaciones es parte de un ensayo clínico bien diseñado que garantiza que el medicamento final será seguro”, explica César Hernández, jefe del departamento de medicamentos de uso humano de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Precisamente por eso se ultiman acuerdos con varias compañías, porque no se sabe cuál conseguirá la vacuna, o cuál lo hará antes.
En total, los acuerdos preliminares de la Comisión Europea —que repartirá dosis de forma proporcional a la población de sus socios— incluyen la compra de 1.205 millones de dosis de estas seis vacunas experimentales contra la covid: 300 millones de la candidata de Oxford y AstraZeneca; otros 300 millones de la desarrollada por la multinacional francesa Sanofi y la británica GSK; 225 millones del prototipo de la biotecnológica alemana Curevac; 200 millones de la opción de la empresa estadounidense Johnson & Johnson, los 200 ya mencionados de BioNTech y Pfizer y 80 millones de dosis de la también estadounidense Moderna.
“Previsiblemente todas ellas llegarán a la firma del acuerdo, como sucedió con la de Oxford, es una negociación similar con todas, en la que se establece una compra anticipada de un volumen de dosis y un plan de entrega de acuerdo a las capacidades de fabricación de las compañías”, explica Hernández.
Al estar en plena fase de ensayos, es imposible cerrar de forma inequívoca fechas. Según este responsable de AEMPS, las primeras dosis de todas ellas están previstas entre finales de este año y mediados del siguiente. AstraZeneca calculaba que la suya estaría lista para diciembre de 2020, pero la parada en los ensayos puede retrasar esta fecha. “Pueden ser horas, días o semanas hasta que un comité científico independiente consiga averiguar a qué se debió el efecto adverso”, añade Hernández.
De las 179 vacunas experimentales contra la covid —34 de ellas con ensayos en humanos—, ocho prototipos ya están en la fase 3. El más avanzado era precisamente el de la Universidad de Oxford, con resultados prometedores en un primer ensayo con 1.000 personas publicado en julio. Los investigadores británicos están llevando a cabo las últimas pruebas con 50.000 personas en el Reino Unido, Brasil, Sudáfrica y EE UU. En este mismo estadio están la de Moderna, la de BioNTech y Pfizer, las chinas de Fosun Pharma y Cansino Biologics y una de fabricación rusa.
La misión de la AEMPS es hacer llegar a Salud Pública un porfolio entre las vacunas que hayan demostrado calidad, seguridad y eficacia. En función de los resultados en los ensayos, se establecerán protocolos para vacunar a la población. Aunque Fernando Simón, director del Centro de Coordinación de Alertas y Emergencias Sanitarias, dijo el lunes que lo primero serían sanitarios y población vulnerable, todo depende de las características que tenga el medicamento (o medicamentos) final. Podría darse el caso de que en las pruebas con miles de sujetos (en la fase 3) se detectasen efectos adversos en personas con determinadas patologías o de edades concretas que impidieran vacunarlas.
El Ministerio de Sanidad ha llegado este miércoles a un acuerdo con las comunidades autónomas, en el seno del Consejo Interterritorial de Sanidad para elaborar esta estrategia de vacunación. Se elaborará de forma conjunta con la opinión de expertos en bioética y de las sociedades científicas. Son los gobiernos regionales los que se tendrá que encargar de tener disponibles todos los materiales, equipos y recursos humanos para la administración de las inmunizaciones. Además, tal y como adelantó el ministro el pasado viernes, se creará un registro con las personas vacunadas para poder realizar un seguimiento.
La investigación de los medicamentos en realidad no concluye cuando están en el mercado. Lo que se conoce como fase 4 consiste precisamente en reportar todos los casos y efectos adversos una vez que se aplican en la población. Esto permite afinar el proceso para detectar consecuencias muy poco frecuentes o en grupos muy concretos que pueden pasar desapercibidas en los ensayos.
Información sobre el coronavirus
- Aquí puede seguir la última hora sobre la evolución de la pandemia
- Así evoluciona la curva del coronavirus en España y en cada autonomía
- Descárguese la aplicación de rastreo para España
Archivado En
- Coronavirus
- Coronavirus Covid-19
- Emergencia sanitaria
- Enfermedades infecciosas
- Sociedad
- Vacunación
- Vacunas
- Política sanitaria
- Inmunología
- Unión Europea
- Prevención enfermedades
- Salud pública
- Medicina preventiva
- Investigación científica
- Industria farmacéutica
- AstraZeneca
- Universidad Oxford
- Pfizer
- Sanofi
- Johnson & Johnson
- Moderna
- Aemps
- Ensayos clínicos
- CanSino Biologics


























































