Las barreras de las farmacéuticas pueden frenar la nueva revolución en la lucha contra el sida
El sector adolece de una gran opacidad en los costes de la I+D, los resultados de los ensayos clínicos o el precio real para el pagador público del desarrollo de medicamentos
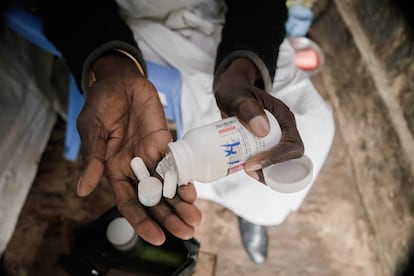
La Estrategia contra el VIH aprobada en 2023 puso como meta reducir las infecciones por VIH a menos de 335.000 casos para 2030. Pero, en 2022, entre 1 y 1,7 millones de personas se infectaron por VIH, según datos de ONUSIDA. Si bien las infecciones se han reducido un 38% desde 2010, alcanzar el objetivo de 2030 supondría reducir en casi un 80% los valores actuales en apenas seis años, triplicando la velocidad de reducción actual. Por ello, priorizar las estrategias de prevención del contagio, como la profilaxis preexposición (PrEP), se hace prioritario.
En los últimos años, la prevención del VIH ha progresado enormemente, con la introducción de formulaciones inyectables de acción prolongada que permiten una mayor adherencia al tratamiento, al reducir la frecuencia de las dosis. Desde el lanzamiento de la PrEP, se ha pasado de una pastilla diaria, a una inyección cada dos meses con el lanzamiento del cabotegravir (CAB-LA). Ahora, un nuevo tratamiento podría revolucionar la PrEP: el lenacapavir (LEN), cuyos prometedores resultados en ensayos clínicos permiten prevenir la infección con tan solo dos inyecciones al año. El lenacapavir ha demostrado una eficacia del 100% en la prevención de nuevos casos de VIH en mujeres cisgénero [que se sienten identificadas con su sexo de nacimiento] en Sudáfrica y Uganda, con superioridad frente a los tratamientos orales y diarios. Además, no requiere ser mantenida en cadena de frío, por lo que facilita su manejo logístico e integración en cadenas de suministro en países con altas temperaturas.
El lenacapavir, con prometedores resultados en ensayos clínicos, podría prevenir la infección con tan solo dos inyecciones al año
A pesar de todas estas ventajas, el acceso a estas herramientas fundamentales de salud pública se enfrenta a numerosos obstáculos, compartidos, en parte, por todo el modelo de innovación y desarrollo farmacéutico. Y es que, como cada vez más evidencia apunta, las prácticas de los sectores comerciales —en concreto de corporaciones transnacionales— son responsables de los malos resultados en salud y en la equidad en salud (lo que se conoce como determinantes comerciales de la salud).
¿Qué podemos aprender de la experiencia pasada en este tipo de productos que nos permita no repetir los mismos errores en el futuro? El caso del cabotegravir nos puede dar una idea del tipo de desafíos complejos e interconectados que impiden que las personas que más los necesitan puedan acceder a estos tratamientos: problemas derivados del monopolio y los precios, regulatorios, o de producción.
El monopolio de la compañía ViiV Healthcare es el factor principal responsable de los elevados precios del CAB-LA, al impedir que otras compañías que pueden fabricar versiones genéricas de este medicamento entren en el mercado. A pesar de que el precio para países de bajos ingresos (alrededor de 180 euros por persona/año) es bastante inferior al que se paga en otros países, sigue siendo inalcanzable para muchos programas nacionales de salud, y se estima que debería ser al menos cuatro veces inferior para ser viable. Estudios independientes han demostrado que el precio de los genéricos, de existir, podría llegar a bajar a 13 euros por persona/año, llegando a ser inferior que la actual PrEP oral.
En el plano regulatorio, los ensayos necesarios para que sus versiones genéricas lleguen al mercado, denominados ensayos de bioequivalencia, retrasarán la entrada de competidores aún más. En 2022, ViiV Healthcare y el Medicines Patent Pool (MPP) —un fondo de patentes fundado por la organización de salud global Unitaid para facilitar el acceso a los medicamentos— firmaron un acuerdo de licencia por el que la compañía permitía a MPP gestionar y utilizar la Propiedad Intelectual del CAB-LA a productores de genéricos para comercializar a precios asequibles el tratamiento en muchos países de rentas medias. Sin embargo, debido a estos ensayos de bioequivalencia, no se espera que las empresas de genéricos puedan comercializar sus productos hasta dentro de tres años.
En 2022, el CAB-LA había sido aprobado para su uso en prevención en solo cuatro países, con solicitudes de comercialización en otros 12. Para 2024, ha sido aprobado en 20 países y existen solicitudes en otros nueve, en gran parte gracias a la presión de la sociedad civil. Solicitar la autorización de comercialización es un paso previo clave para la disponibilidad del medicamento, y, por lo tanto, elemento clave del acceso ante situaciones de monopolio.
La transparencia es un elemento esencial para tener cadenas de suministro resilientes que contribuyan a la mejora de la salud pública. Lamentablemente, la transparencia no define al actual ecosistema farmacéutico, que se cimenta sobre una gran opacidad en los costes de la investigación y desarrollo (I+D), los resultados de los ensayos clínicos o el precio real para el pagador público. En el caso del CAB-LA, la falta de transparencia sobre la capacidad de producción y la cadena de suministro limita la capacidad de respuesta ante una demanda global creciente. Y como hemos visto en la respuesta a la covid-19, a la mpox (forma fulminante de la viruela del mono) o al ébola, en situaciones de demanda creciente, los países de rentas medias y bajas son los últimos en poder acceder al tratamiento.
La transparencia es un elemento esencial para tener cadenas de suministro resilientes que contribuyan a la mejora de la salud pública
Estas lecciones aprendidas con el CAB-LA nos dan algo de claridad sobre el incierto futuro del acceso al lenacapavir. La compañía que tiene la propiedad intelectual de este último, Gilead, no tiene aún una estrategia clara de acceso global. El entramado de patentes que rodean al producto impedirá la entrada de ningún competidor genérico hasta el vencimiento de su última patente, en agosto de 2038 (fecha que puede ser ampliada según las leyes que regulan las diferentes protecciones y exclusividades de los medicamentos en el mercado). Ante esta perspectiva, es crítico que la compañía conceda licencias voluntarias para incrementar el acceso a genéricos. Para esto, el acuerdo que establezca con el Medicines Patent Pool debería incluir al mayor número de países posibles, siguiendo criterios de salud pública y no únicamente de maximización del beneficio.
Idealmente, estos acuerdos de licencia deben emplazarse dentro de una estrategia de acceso global más amplia: registros rápidos del producto a nivel global, transparencia a lo largo de la cadena de suministro y precios accesibles para los diferentes sistemas de salud y organizaciones que quieran incorporar estos productos. Sin embargo, las medidas voluntarias tienen un impacto muy limitado, como vimos durante la covid-19. Así que, de cara al futuro, ¿qué más podemos hacer?
En la actualidad hay iniciativas muy interesantes impulsadas por [la organización internacional] UNITAID, en las que se están desarrollando formulaciones de acción prolongada no solo para el VIH, sino para malaria, tuberculosis o hepatitis C, para que las innovaciones producidas sean accesibles. Además, llevan a cabo proyectos de financiación para introducir CAB-LA en Brasil y Sudáfrica para impulsar el escalado global.
Aparte de estas acciones, existen más herramientas para cambiar el statu quo inicial. Una de ellas está recogida legalmente en los Aspectos de la Propiedad Intelectual relacionados con el Comercio: las licencias obligatorias. Con ellas se obliga a las compañías a conceder licencias de patentes para producir genéricos. Esto es lo que hizo Colombia al emitir una licencia obligatoria para acceder a versiones genéricas de dolutegravir, un tratamiento contra el VIH. En el caso de las formulaciones de acción prolongada, incluso si se diese esta situación, lo más probable es que en el corto o medio plazo no fuéramos a ver los resultados materializados, ya que estos son procesos generalmente muy lentos. A pesar de esto, estas medidas deben ser tenidas en cuentas por los gobiernos para garantizar la salud pública, ya que a veces la propia amenaza de la licencia obligatoria tiene efectos de reducción de precio.
Estas son soluciones a posteriori, pero no ofrecen alternativas para repensar el modelo de tal manera que la innovación sea accesible globalmente por defecto, una parte integral de las políticas, actuando lo antes posible y lo más arriba posible de la corriente para producir el mayor impacto. Más allá de la reforma necesaria del actual sistema actual de propiedad intelectual, existen oportunidades de actuar sobre el marco regulatorio de las leyes farmacéuticas, mejorando la transparencia y el acceso global.
Una oportunidad para esto es la actual revisión de la legislación farmacéutica europea, donde estos principios deberían establecerse como piedras angulares y no como excepciones. Por ejemplo, condicionando los ingentes incentivos que se otorgan actualmente a las compañías farmacéuticas a través de la financiación pública —sin esperar ningún retorno público a cambio— a compromisos vinculantes de desarrollo e implementación de planes de acceso global como los arriba mencionados.
Esta visión de la política regional como determinante político de la salud global es aún escasa entre los decisores políticos, que limitan el marco de análisis a la clave nacional o europea. Sin embargo, es necesario que actuemos en todos los frentes para alcanzar las metas que la comunidad internacional se propuso de cara a 2030. Como ya comunicamos al Consejo de la UE recientemente, “proveer acceso y suministro adecuados a los medicamentos es el estándar por el cual las compañías farmacéuticas deberían ser evaluadas, no un comportamiento a ser recompensado”.
Puedes seguir a Planeta Futuro en X, Facebook, Instagram y TikTok y suscribirte aquí a nuestra ‘newsletter’.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.




























































