El retorno de los virus devoradores de bacterias
Los fagos llevan tiempo salvando la vida de personas con infecciones inmunes a los antibióticos. En España, los investigadores piden que se permitan estos tratamientos para pacientes sin más opciones

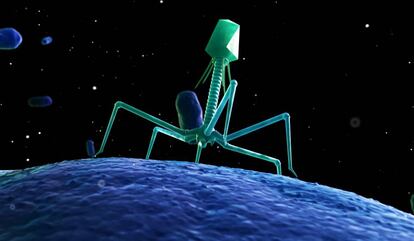
Hace cien años, algunas de las grandes empresas farmacéuticas vendían preparados a base de virus para tratar de combatir las infecciones bacterianas que hacían estragos cuando aún no había antibióticos. Felix d’Herelle, un médico canadiense que bautizó a estos microorganismos como bacteriófagos, devoradores de bacterias, los utilizó para tratar con cierto éxito a enfermos de cólera o peste bubónica y creó medicamentos virales que después comercializó L’Oréal. En un estudio con enfermos de cólera realizado en el Punjab indio en 1927, cuando aún formaba parte del imperio británico, el 92% de los pacientes tratados con fagos se salvaron frente al 37% de los que no recibieron tratamiento.
Algunos resultados eran prometedores, pero las dificultades para aislar los virus y tratarlos para convertirlos en medicamentos hizo que muchos de estos productos fuesen de baja calidad y poco o nada útiles. Además, en esos años se estaba produciendo una auténtica revolución médica. La aparición de los antibióticos, mucho más eficaces y sencillos de producir a escala industrial, hizo que muchos pensasen que las infecciones ya no serían un problema para la humanidad y los fagos se abandonaron como terapia en Occidente.
Las bacterias resistentes a los antibióticos matan a más de 30.000 personas cada año solo en Europa
La situación ha cambiado y los virus matabacterias vuelven a por una segunda oportunidad. Las bacterias se han adaptado al uso masivo de antibióticos con una versatilidad asombrosa. El Centro Europeo para la Prevención y el Control de Enfermedades calcula que solo en Europa las bacterias resistentes a los antibióticos matan a más de 30.000 personas cada año y la ONU ha impulsado un acuerdo mundial para combatir una amenaza global que considera apremiante. Hace unos días, la curación de una adolescente británica presentó al mundo este tipo de terapias. Isabelle Holdaway, desahuciada por una infección inmune a los antibióticos, había salvado la vida gracias a un tratamiento con fagos modificados genéticamente.
Esta misma semana, la prensa belga anunciaba otro éxito del tratamiento de una infección con virus bacteriófagos. Un equipo del Hospital Universitario Saint-Luc, en Bruselas, salvó la vida de un bebé que había nacido con una deficiencia en el hígado que requirió un trasplante. Tras la operación, el pequeño sufrió una infección en el hígado y en la sangre que no respondió a los antibióticos. Los médicos decidieron aplicar un tratamiento con fagos que duró 85 días, el tiempo necesario para entrenar a los fagos para que detectasen y destruyesen la infección concreta que sufría el niño.
Los antibióticos son un producto químico que mata a las bacterias bloqueando algún proceso fundamental para su supervivencia. “Tienen la ventaja de que actúan contra una diana que puede estar en una especie bacteriana o en todas las bacterias”, explica Daniel López, experto en superbacterias del Centro Nacional de Biotecnología del CSIC. Esto permite la existencia de los antibióticos de amplio espectro, que pueden ayudar a combatir una infección aunque no se sepa exactamente qué bacteria la ha causado.
Los fagos matan a las bacterias porque les inyectan su ADN para reproducirse y después las revientan por dentro. Cada virus infecta a bacterias de cepas muy concretas y eso tiene ventajas e inconvenientes. “En el caso de la chica británica, fue necesario probar una colección de más de 10.000 fagos para encontrar los que pudiesen ser útiles”, apunta López. “Eso no te permite generar un tratamiento rápidamente”, concluye. En el lado positivo, el tratamiento es muy específico, es menos probable que genere bacterias superresistentes y no daña a los microbios beneficiosos de nuestro organismo.
Por ahora, como sucedió con Holdaway, solo se recurre a los fagos cuando se han agotado las soluciones convencionales. Algunos enfermos recurren incluso al peregrinaje a Tiblisi, Georgia. Allí, en el centro de investigación fundado por George Eliava, un discípulo de D’Herelle que acabó fusilado por enamorarse de una mujer a la que deseaba Lavrenti Beria, el jefe de la policía política de Stalin, se continuó con la investigación sobre fagos para aplicaciones médicas cuando se abandonó en occidente.
Para poder aplicar los fagos como terapia compasiva para quienes no tienen otra opción, las agencias reguladoras deben dar su visto bueno. Las dudas sobre su eficacia basadas en los resultados del pasado o el riesgo de que una mala purificación de los fagos provoque una reacción inmune letal dificultan estos permisos. Pilar García, coordinadora de la red española de investigadores en bacteriófagos, explica que “en España no se está aplicando este tratamiento compasivo” y se van “a reunir con la Agencia Española del Medicamento para hacerlo posible”. “Ahora, uno de los productos desarrollados en mi instituto se están purificando para dárselos a pacientes en un hospital de Lyon, y también nos los han pedido desde otros países como Suiza”, señala García, que es investigadora del Instituto de Productos Lácteos de Asturias del CSIC, en Villaviciosa. “Hay gente con infecciones sin tratamiento cerca de nosotros y sería una pena que se desperdiciase esta posibilidad de ayudarles”, concluye.
La red española de investigadores en bacteriófagos se va a reunir con la Agencia Española del Medicamento para debatir la aprobación de estos tratamientos
En el mercado ya hay tratamientos a base de bacteriófagos para acuicultura, en un ámbito como el de la salud animal que ha sido un entorno donde el uso irresponsable de antibióticos ha supuesto un entrenamiento excelente para las superbacterias. La empresa neerlandesa Micreos produjo la primera endolisina para uso humano. Estas proteínas, utilizada por los fagos para hacer eclosionar la bacteria desde su interior y salir al mundo, se utilizan en el caso del fármaco Staphefekt para atacar a la bacteria Staphylococcus aureus, responsable de enfermedades inflamatorias de la piel como el eczema. Micreos también tiene productos con proteínas específicas contra Listeria, Salmonella y Escherichia coli para seguridad alimentaria.
En España, la empresa Ikan Biotech, con sede en Pamplona, también está intentando desarrollar este tipo de “enzibióticos” a partir de las proteínas que producen los fagos para reventar las bacterias. Roberto Díez-Martínez, fundador de la compañía, explica cómo recogen bacterias del subsuelo que nunca hayan tenido contacto con humanos para buscar en ellas bacteriófagos que puedan matar a bacterias multirresistentes. “Tenemos unas 15.000 bacterias en nuestra librería. De ellas, hemos analizado un 10% y hemos obtenido 408 fagos de los que tras un cribado tenemos 72 que son positivos para patógenos humanos. Ahora, buscamos aquellos que maten a los cuatro organismos prioritarios y otros que han generado multirresistencia”, indica.
El investigador considera que el desarrollo de este tipo de antibacterianos será lento por la complejidad del proceso, pero también porque para las empresas farmacéuticas, de momento, es más rentable producir antibióticos por los métodos químicos tradicionales. Pero el número de bacterias resistentes a los antibióticos de último recurso, como el que casi mata a Isabelle Holdaway, aumenta, y serán necesarias todas las alternativas posibles. Los virus devoradores de bacterias pueden dar esperanza a miles de enfermos.
Puede escribirnos a daniel@esmateria.com o seguir a Materia en Facebook, Twitter, Instagram o suscribirse aquí a nuestra newsletter.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.


























































