Fotografiar antes de destruir
Los pulsos ultracortos y muy intensos de un láser de rayos X obtienen imágenes inéditas de proteínas y virus
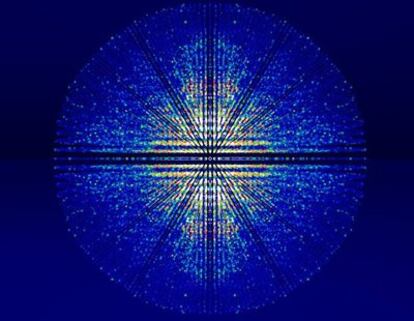
Utilizar los pulsos increíblemente intensos y cortos de un láser de rayos X para fotografiar materiales biológicos con alta resolución ha sido un sueño para los investigadores desde hace al menos una década. Ahora un grupo internacional de científicos ha demostrado que esto es posible en una fuente de luz láser del laboratorio SLAC en California. Han obtenido imágenes del complejo de proteínas Fotosistema 1 y de partículas del mimivirus. Este método, todavía experimental, inicia una nueva forma de obtener estructuras moleculares de proteínas y virus sin la necesidad de disponer antes de buenos cristales, lo que simplificará y acelerará mucho el proceso.
Es un caso curioso, en el que se ha ido comprobando paso a paso una hipótesis publicada hace 10 años, que se conoce como difracción antes de la destrucción. Entonces se sugirió que los pulsos de femtosegundos (millonésima parte de un nanosegundo) de duración de un láser de electrones libres podrían proporcionar dosis de rayos X suficientemente breves e intensas para obtener información útil de la estructura (imágenes) antes de que produjeran daños, es decir, antes de que la muestra se vaporizara como plasma, el cuarto estado de la materia.
Los investigadores han podido usar muestras no útiles anteriormente, como una partícula de virus y nanocristales de proteínas, tan pequeños que no se pueden ver con un microscopio óptico.
La difracción por rayos X, recuerdan los investigadores, ha sido una herramienta imprescindible para determinar estructuras en todas las ciencias, pero su éxito ha dependido de la disponibilidad de muestras cristalinas de un tamaño suficiente. Es famoso el ejemplo de la estructura del ADN.
Con las fuentes de rayos X convencionales, aumentar la dosis de radiación para compensar que se disponga de un cristal pequeño puede dañar mucho la estructura antes de que se pueda grabar el patrón de difracción. Este problema ha sido especialmente grave con algunos materiales biológicos que pueden resultar muy difíciles, o imposibles, de cristalizar.
Los dos trabajos, que publica Nature, utilizan nuevos sistemas de inyección de las muestras. En el primero, dirigido por Henry Chapman, del instituto alemán DESY, se usó un chorro de agua para transportar un flujo de nanocristales, y en el segundo, dirigido por Janos Hajdu (Universidad de Uppsala, Suecia), se expuso un chorro de partículas de virus en aerosol y se mostró que se puede obtener suficiente información de estos objetos no cristalinos antes de que resulten dañados.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.































































