
El reto de afrontar el cáncer de mama: guía práctica para conocer los diferentes tipos, diagnósticos y técnicas avanzadas
El cáncer de mama es una enfermedad plural, con nombre propio y muchos apellidos. En las últimas décadas, la oncología se ha volcado en buscarlos y categorizarlos para desarrollar tratamientos de precisión que mejoren la calidad de vida del paciente y prolongar la supervivencia.
El cáncer de mama es una enfermedad heterogénea con muchos, muchísimos, apellidos. Los avances oncológicos de las últimas décadas han hecho que este nombre genérico, que tan solo se refiere a la zona del cuerpo en la que se origina, se nos quede corto. “Hoy sabemos que es un conjunto de entidades clínicas y patológicas que tienen diferencias biológicas, tan relevantes, que hacen que el tratamiento sea completamente diferente entre unos casos y otros”, subraya el doctor César A. Rodríguez, jefe del servicio de Oncología Médica del Hospital Universitario de Salamanca y presidente de la Sociedad Española de Oncología Médica (SEOM).
El diagnóstico ya no se reduce a tumores benignos o malignos, en un estadio precoz o más o menos avanzado. La medicina aborda cada caso desde una perspectiva más amplia, que tiene en cuenta sus características clínicas, histológicas y moleculares. “Esto ha venido de la mano de un mayor conocimiento de la genómica en el cáncer de mama, que ha permitido clasificar los tumores en lo que llamamos subtipos intrínsecos”, apunta el experto; lo que está permitiendo desarrollar diagnósticos más sofisticados y, en consecuencia, tratamientos más acertados.
«Hace apenas 10 años, para decidir si una paciente operada de cáncer de mama debía recibir quimioterapia, nos basábamos en algo tan grosero como el tamaño del tumor y la presencia o no de ganglios en las axilas. Lo que ocurría es que con frecuencia estábamos administrando quimioterapia a pacientes que nunca la hubieran necesitado porque biológicamente esos tumores no eran tan agresivos o tan quimio-sensibles», recuerda el doctor A. Rodríguez. La aplicación de la genómica ha impulsado el cambio hacia estrategias de desescalada, donde ya no se pregunta quién necesita quimioterapia, sino quién no lo necesita para curarse.
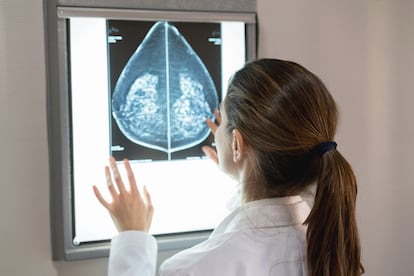
Estamos en estrategias de desescalada: seguimos usando quimioterapia, pero hemos aprendido mucho más a quién no hay que dársela.Doctor César A. Rodríguez, jefe del servicio de Oncología Médica del Hospital Universitario de Salamanca
Asegura que incluso en casos de cáncer metastásicos, cuando el paciente ha recaído, su uso también se está retrasando, “porque tenemos estrategias de nuevas terapias biológicas basadas en biomarcadores específicos que permiten agotar otras vías de tratamiento antes de llegar a la quimioterapia clásica. Empleamos pequeñas moléculas, tratamientos biológicos o, en algunos escenarios, inmunoterapia”, enumera.
¿Qué tipos de cáncer de mama existen?
El cáncer de mama se divide, según su clasificación molecular, en tres grandes grupos. Los Tumores Luminales, que dependen de las hormonas (estrógenos o prostegerona) para su crecimiento, representan en torno al 25% y el 50% de los cánceres de mama. Los Tumores HER2 positivo se caracterizan por tener altos niveles del receptor de factor de crecimiento epidérmico tipo 2 (HER2, por sus siglas en inglés), una proteína que propicia la aparición de células cancerosas; mientras que los terceros, los Tumores Triple Negativo, que no expresan receptores de HER2 ni hormonas, son considerados más agresivos y difíciles de tratar. «Han tenido mal pronóstico porque teníamos muy pocas estrategias y tratamientos inespecíficos, pero incluso dentro de este subgrupo las cosas están cambiando y empezamos a identificar biomarcadores», subraya el doctor, un concepto que se repite a lo largo de la conversación.
Los biomarcadores son los apellidos del cáncer: “Es una alteración biológica en el tumor, como la mutación de un gen o la expresión de una proteína, que te lleva a un tratamiento específico”, puntualiza el experto. Toda la toma de decisiones de un cáncer de mama, tanto en estadios precoces como avanzados, se basa en este catálogo de biomarcadores, capaz de conocer las características del tumor y predecir cómo van a responder a un tratamiento. “Es lo que llamaríamos la medicina de precisión personalizada”.
¿Cuándo se debe realizar una mamografía?
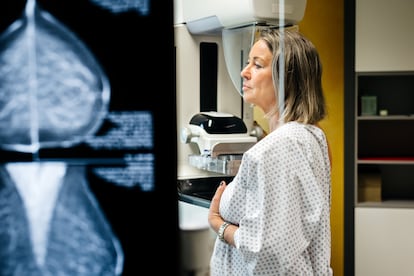
El cáncer de mama, desde 2021, es el tumor más diagnosticado en todo el mundo. La Sociedad Española de Oncología Médica (SEOM) prevé que en 2024 se diagnosticarán 36.395 nuevos casos de cáncer de mama. Las cifras aumentan anualmente, pero también lo hace la supervivencia, con un índice a cinco años superior al 85%. Que haya lugar para el optimismo se debe, además de las innovaciones, a la eficacia de los cribados en la detención precoz. «La mamografía es la prueba más conocida y la única que ha demostrado que puede aportar beneficios a nivel poblacional», apunta el doctor A. Rodríguez.
Tradicionalmente, se recomendaba que las mujeres entre los 50 y los 70 años, se realizaran una mamografía cada dos años. Debido a la incidencia en edades cada vez más tempranas —el doctor señala factores como el estilo de vida, la baja natalidad o la maternidad tardía—, así como el aumento de la esperanza de vida, la Comisión Europea y el Sistema Nacional de Salud han ampliado el rango, desde los 45 hasta los 74 años. “Hay factores que a nivel poblacional son difíciles de corregir, como tener hijos a edades más tempranas o dar una lactancia materna prolongada, cuando no hay posibilidad de hacerlo, por ejemplo, por la baja laboral; pero sí podemos incidir en factores que a nivel individual podemos compensar: una dieta saludable, ejercicio físico regular, bajar el consumo de alcohol o evitar la obesidad”.
¿Sirve la autoexploración mamaria? Aunque no puede ni debe sustituirse por una mamografía, para el experto, puede ser útil para detectar signos de alarma. “Fundamentalmente son muy clásicos: la aparición de un bulto que previamente no se encontraba, el enrojecimiento de la mama que no mejora en un plazo muy corto de tiempo, una secreción inadecuada por el pezón, una retracción de la piel… Todos aquellos signos que supongan un cambio significativo en la mama deben ser consultados con el médico”.
¿Y si existen antecedentes familiares?
Conocer la existencia de una mutación hereditaria es una información de gran valor para una familia. Las mutaciones en genes como BRCA1 o BRCA2 –responsables de entre el 20% y 25% de los cánceres hereditarios, entre otros– aumentan el riesgo a presentar cáncer de mama u ovario entre las mujeres, especialmente entre las más jóvenes. O, en el caso de los hombres, de próstata. “No olvidemos que el 1% de los cánceres de mama afectan a los varones. Son más de 350 hombres al año en España, sobre los que se ha incidido muy poco”, insiste A. Rodríguez. Tener antecedentes familiares, sin embargo, no significa que un cáncer sea hereditario.
Tampoco se realizan pruebas genéticas a todo el mundo. Ante la sospecha, las unidades de consejo genético, un equipo multidisciplinar formado por asesores genéticos, oncólogos, médicos o cirujanos, entre otros; se encargan de estudiar la carga genética para valorar si se cumplen los criterios para hacer la prueba genética. “Si se establece que de verdad hay un riesgo, lo que se hace es obtener una muestra de sangre, preferiblemente de quien ya ha tenido el tumor, porque las mutaciones están presentes en la línea germinal, no hay porque ir al tumor”. Las búsquedas también se han ampliado, abriendo el abanico a genes como el ATM, el CHEK2, el TP53 o el PALB2. No son tan frecuentes, pero sí, relevantes a la hora de prevenir con el tratamiento.

Alrededor del 5% y el 10% de los cánceres de mama son hereditarios, según datos de la Sociedad Española de Oncología Médica, lo que afecta a las estrategias de tratamiento
¿Qué técnica es más adecuada a mi diagnóstico?
“El cáncer de mama es una enfermedad dinámica”, asegura el doctor César A. Rodríguez. “A medida que sometemos el tumor a un tratamiento, pueden aparecer modificaciones en su biología que hagan que el tratamiento en un momento A ya no sea válido en un momento B”. El desarrollo de técnicas de diagnóstico avanzado, como la biopsia líquida y la secuenciación masiva, han supuesto un cambio significativo, permitiendo un seguimiento más personalizado y dirigido a las necesidades de cada momento.
“La biopsia líquida nos permite con una simple muestra de sangre lo mismo que antes teníamos que hacer mediante una punción, en un órgano a veces complejo o inaccesible: encontrar el ADN circulante de las células tumorales, lo que me va a permitir analizar los cambios genómicos y saber cuál es el mejor tratamiento para ese tumor en ese momento concreto”, apunta el doctor. Sumado a la secuenciación masiva, que permite analizar centenares de mutaciones genéticas de forma rápida, la oncología trabaja con un panel mucho más amplio “de puntos potenciales sobre los cuales podemos obtener un resultado terapéutico”. En la actualidad, la aplicación de ambas técnicas se reserva para casos de cáncer metastásico.
¿Cuál son los principales retos?
El cáncer de mama sigue siendo la primera causa de muerte entre las mujeres españolas. “Esto es debido a que la enfermedad en el momento que recae, y lo hace con metástasis, en la inmensa mayoría de los casos deja de ser curable”, apunta el experto. “La buena noticia es que precisamente el desarrollo de nuevos tratamientos más específicos y menos tóxicos está permitiendo aumentar muchísimo la supervivencia y hacerlo con mucha mejor calidad de vida que en décadas pasadas”.
Para alcanzar algún día la cronificación del cáncer, para el doctor César A. Rodríguez, hay dos aspectos fundamentales. Por un lado, exige que la toma de decisiones en el tratamiento de un cáncer siempre se realice por un equipo multidisciplinario en el que participan todos los especialistas implicados en el diagnóstico, tratamiento y seguimiento de la enfermedad. “Está demostrado que mejora el pronóstico y el resultado de los tratamientos”. Por otro lado, pone el foco en las secuelas físicas y emocionales de la enfermedad, reclamando planes integrales de atención de los largos supervivientes de cáncer. “Es absolutamente necesario para que la enfermedad no solo se cure, sino que no deje secuelas en todas las dimensiones de la vida de estas mujeres”.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.







































