Los peligros de la edición genómica
Los líderes de la genética mundial alertan contra la “reacción en cadena” que permite propagar genes por toda una población

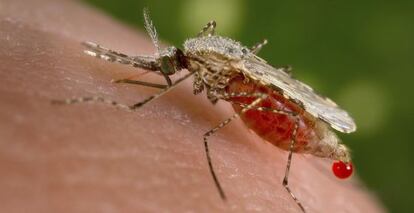
Entre las aplicaciones de la revolucionaria técnica de edición genómica (crispr/cas, cuyas inventoras recibieron el último Príncipe de Asturias), hay una que ha puesto los pelos de punta a los propios genetistas que la usan. Se llama “reacción en cadena genética”, o “impulso genético” (gene drive), y causa la propagación de modificaciones genéticas no ya entre las células de un individuo, sino por todos los individuos de una población. Se acaba de demostrar en moscas, el organismo modelo de la genética por excelencia. Pero la gran virtud de crispr/cas es precisamente que sirve para cualquier especie, incluida la nuestra.
Son fines nobles, pero mientras se desarrollan estos métodos, existe el riesgo obvio de que los insectos manipulados se escapen al campo y armen una catástrofe ecológica
Los científicos, entre ellos muchos líderes del campo, recomiendan que estos experimentos se sometan a una batería de medidas de confinamiento que impida su escape accidental y propagación por la naturaleza. Estos 26 investigadores hacen públicas sus recomendaciones en Science. Las posibles aplicaciones en humanos son por el momento ciencia ficción, aunque puede ser un buen ejercicio para novelistas imaginar alguna de ellas. Por ejemplo, en manos de un psicópata rabioso o de un político canalla.
El impulso genético (gene drive) es en realidad un fenómeno que existe en la naturaleza, y hay científicos que piensan que es importante para la especiación, o generación de nuevas especies en la evolución. Nuestras células tienen dos copias de cada gen, y cada una tiene un 50% de probabilidad de pasar a la descendencia. Pero hay genes que manipulan ese juego justo y aumentan sus probabilidades. A lo largo de las generaciones, incluso una pequeña ventaja puede bastar para que ese gen se imponga en la población.
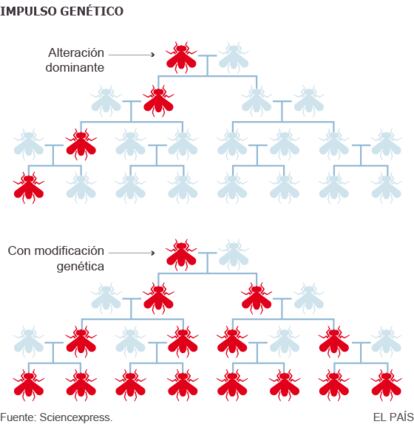
Y lo que ofrece la técnica de edición genómica crispr/cas al gen tramposo no es una pequeña ventaja, sino cuatro ases en la manga (véase figura). El gen artificial introducido por un investigador en el organismo sigue activo, y es capaz de convertir al gen natural que tiene enfrente en una copia de sí mismo. El proceso no para nunca, y es tan eficaz que propaga el gen artificial por toda la población en pocas generaciones. De ahí su apodo de “reacción en cadena. El experimento en la mosca es obra de Valentino Gantz y Ethan Bier, de la Universidad de California en San Diego, y se publicó en marzo. Cabe mencionar que Gantz y Bier son dos de los 26 científicos que ahora firman la nota de alerta.
El objetivo de los científicos interesados en la reacción en cadena es sensato. Quieren diseñar métodos eficaces para alterar la genética de las poblaciones naturales de, por ejemplo, los mosquitos que transmiten la malaria y otras enfermedades que son un grave problema de salud pública en los países en desarrollo.
Los científicos, entre ellos muchos líderes del campo, recomiendan que estos experimentos se sometan a una batería de medidas de confinamiento que impida su escape accidental y propagación por la naturaleza
También se proponen erradicar a las especies invasivas que se han introducido –por error, descuido o un mal evaluado interés económico— en ecosistemas que pueden sucumbir a ellas. Y controlar las plagas más dañinas para la agricultura, como una alternativa al uso extensivo de pesticidas que dañan al medio y a los polinizadores naturales como abejas y abejorros.
Son fines nobles, pero mientras se desarrollan estos métodos, existe el riesgo obvio de que los insectos manipulados se escapen al campo y armen una catástrofe ecológica.
“Uno de los grandes éxitos de la ingeniería es el desarrollo de sistemas de seguridad”, dice George Church, jefe de biología sintética del Instituto Wyss de Ingeniería Inspirada en la Biología de la Universidad de Harvard, “como, por ejemplo, redondear las esquinas de los objetos o la invención de los airbags para el coche; en la ingeniería biológica queremos emular ese proceso de seguridad. Church, que es un genetista famoso por su audacia, ha intervenido en el desarrollo de sistemas de bioseguridad para los sistemas de edición genómica, incluida la reacción en cadena".
Quieren diseñar métodos eficaces para alterar la genética de las poblaciones naturales de, por ejemplo, los mosquitos que transmiten la malaria y otras enfermedades que son un grave problema de salud pública en los países en desarrollo
El grupo de los 26 ha sido coordinado por Church, su colega en el Wyss Kevin Esvelt y el biólogo del desarrollo Ethan Bier, de la Universidad de California en San Diego. Además de llamar la atención de otros científicos interesados en la reacción en cadena genética, proponen ya una serie de medidas concretas que constituyen una batería de barreras de confinamiento para los organismos manipulados. También hacen una llamada a la transparencia informativa y la discusión pública.
Al haber llegado aquí, el lector ya es parte de esa campaña.
Tu suscripción se está usando en otro dispositivo
¿Quieres añadir otro usuario a tu suscripción?
Si continúas leyendo en este dispositivo, no se podrá leer en el otro.
FlechaTu suscripción se está usando en otro dispositivo y solo puedes acceder a EL PAÍS desde un dispositivo a la vez.
Si quieres compartir tu cuenta, cambia tu suscripción a la modalidad Premium, así podrás añadir otro usuario. Cada uno accederá con su propia cuenta de email, lo que os permitirá personalizar vuestra experiencia en EL PAÍS.
¿Tienes una suscripción de empresa? Accede aquí para contratar más cuentas.
En el caso de no saber quién está usando tu cuenta, te recomendamos cambiar tu contraseña aquí.
Si decides continuar compartiendo tu cuenta, este mensaje se mostrará en tu dispositivo y en el de la otra persona que está usando tu cuenta de forma indefinida, afectando a tu experiencia de lectura. Puedes consultar aquí los términos y condiciones de la suscripción digital.


























































