“Los escándalos del pasado muestran la debilidad de las leyes”
La eurodiputada británica Glenis Willmott encabeza la nueva ofensiva de la Eurocámara para proteger a los consumidores frente a los abusos de la industria médica


La eurodiputada Glenis Willmott lidera la lucha del Parlamento Europeo por endurecer la legislación sobre los dispositivos médicos. En juego está tranquilizar a millones de ciudadanos comunitarios sobre las prótesis e implantes que introducen en sus cuerpos. Hay precedentes que asustan: unas 300.000 mujeres de 65 países fueron víctimas de los implantes de pecho fraudulentos comercializados entre 2001 y 2010 por la empresa francesa Poly Implant Prothèse (PIP). La compañía utilizó silicona industrial no homologada. El escándalo provocó la quiebra de la entidad en 2011. Un año después, la alarma llegó por las prótesis de cadera ASR que Johnson&Johnson retiró del mercado después de que se demostrara que eran defectuosas. La Eurocámara quiere evitar con una nueva ley que casos así vuelvan a repetirse sin ahogar a las empresas en un mar de trámites. Willmott, miembro del Partido Laborista británico de 66 años y eurodiputada desde 2006, ha sido la autora de la ponencia sobre la ley.
Pregunta. ¿Cómo cambiará la nueva ley la vida de los europeos?
Respuesta. Hemos endurecido los requisitos para sacar al mercado dispositivos médicos. Por primera vez, productos estéticos como los implantes de pecho deberán seguir las mismas leyes y adaptarse a las normas de seguridad de otras prótesis médicas. Con esta norma, las pruebas previas a su salida al mercado son más estrictas y habrá controles adicionales para aquellos dispositivos considerados de alto riesgo. Los cambios no afectarán a la forma en que los pacientes usan los dispositivos, pero aumentará la confianza en que los que llegan al mercado son seguros. También habrá mucha más información para los pacientes: todo aquel que tenga un dispositivo implantado recibirá una tarjeta; se publicarán los resultados de todas las investigaciones clínicas previas a su salida al mercado, y si hay razones para creer que un paciente ha sido perjudicado por un dispositivo, el fabricante tendrá que informar de ello al resto de usuarios.
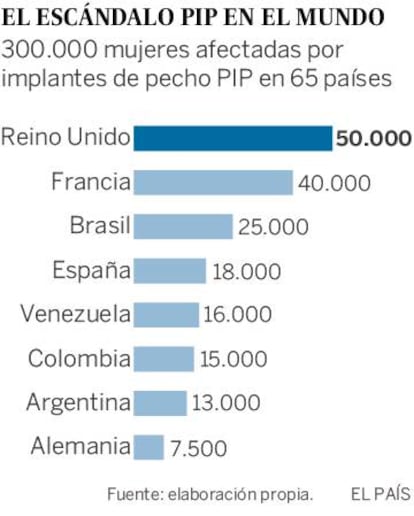
P. Con la nueva ley, ¿será imposible que se repitan fraudes como el de los implantes de pecho PIP?
R. Por desgracia nunca puedes asegurar que es imposible que este tipo de casos sucedan, pero será mucho menos probable. Las reglas para los organismos de certificación, que tienen la responsabilidad de autorizar los dispositivos médicos que salen al mercado, serán más estrictas. El personal que lleva a cabo las evaluaciones deberá estar debidamente cualificado y realizará auditorías a los fabricantes, incluyendo la inspección de muestras de dispositivos, por lo que si se repitiera un caso de fraude como el de PIP, se descubriría rápidamente. Además, todos los productos tendrán un número único de identificación y los pacientes recibirán una tarjeta con esa cifra, así que sabremos inmediatamente qué pacientes lo llevan; En el caso de PIP, muchas mujeres no sabían la marca de su implante, y por tanto no saben todavía si están afectadas.

P. ¿Cuándo entrarán en vigor las nuevas leyes?
R. La regulación entrará en vigor este año, pero habrá un período de transición de tres años. Aunque queremos que las nuevas normas se apliquen lo antes posible, hay que reconocer que hay muchos nuevos requisitos para fabricantes, organismos de certificación y autoridades nacionales, y que necesitarán un tiempo para adaptarse.
P. ¿Por qué no se ha hecho una ley así años atrás?
R. La primera propuesta de la Comisión Europea fue en 2012, y el Parlamento Europeo adoptó su posición en 2013, pero para iniciar la negociación tuvimos que esperar hasta que los Veintiocho Estados de la UE llegaran a un acuerdo. Es un asunto muy técnico, y aunque queríamos que estuviera listo cuanto antes, también queríamos asegurarnos de que se hacía bien.
P. ¿Cuáles han sido los puntos más polémicos?
R. Los escándalos del pasado muestran la debilidad de las actuales leyes, por lo que hemos buscado endurecer las reglas para asegurar que todos los dispositivos que salen al mercado sean seguros. Al mismo tiempo, no queríamos crear trabas administrativas innecesarias que frenen la innovación de la industria, y creo que la nueva ley tiene el equilibrio justo. No puedes jugar con la seguridad y para mí el examen previo a la salida al mercado de los productos de alto riesgo ha sido un punto particularmente importante.
P. ¿Las víctimas de escándalos como los implantes de pecho fraudulentos PIP se beneficiarán de las nuevas normas?
R. Sé que muchas mujeres fueron víctimas de este fraude, y que aún hay muchas que no saben si están entre las afectadas, lo cual es algo verdaderamente horrible. Desafortunadamente, no podemos legislar retroactivamente ni podemos volver atrás en el tiempo, pero la nueva ley debería hacer mucho más difícil que un caso como ese se repita en el futuro.